- Жесткость воды. Мягкая вода. Жесткая вода. Перевод единиц (градусов) жесткости воды. Нормы жесткости воды. Таблицы значений жесткости воды. Умягчение воды. Как убрать жесткость воды.
- Жесткость воды. Мягкая вода. Жесткая вода. Перевод единиц (градусов) жесткости воды. Нормы жесткости воды. Таблицы значений жесткости воды. Умягчение воды. Как убрать жесткость воды.
- Нормы жесткости воды — в 99,99% случаев речь идет о временной жесткости, данные ВСТ:
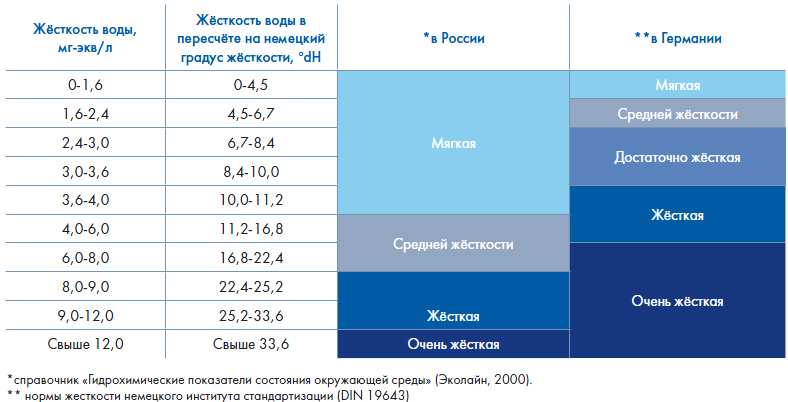
- Сравнение принятных норм жесткости воды в РФ и Европе (Германии), данные Эколайн:
- Жесткость воды в некоторых городах мира — данные МВК — неизвестной достоверности 🙂
- Нормативные требования и рекомендации
- Перевод единиц и градусов жесткости воды — в 99,99% случаев речь идет о временной жесткости:
- Методы устранения жесткости воды
- Что такое жесткость воды и как ее определить
- Жесткость в питьевой воде
- Какие соли обуславливают жесткость природной воды, откуда они берутся
- От чего зависит присутствие соли жесткости в воде
- Классификация воды с солями жесткости
- Нормы жесткости для воды
- Предельно допустимое содержание солей жесткости в воде
- Нормы жесткости для питьевой воды
- Шкала жесткости
- Нормы жесткости для технической воды
- Как определить жесткость воды
- Измерение жесткости воды
- Как определить жесткость воды по формуле
- Как понизить жесткость в питьевой воде
Жесткость воды. Мягкая вода. Жесткая вода. Перевод единиц (градусов) жесткости воды. Нормы жесткости воды. Таблицы значений жесткости воды. Умягчение воды. Как убрать жесткость воды.
Жесткость воды. Мягкая вода. Жесткая вода. Перевод единиц (градусов) жесткости воды. Нормы жесткости воды. Таблицы значений жесткости воды. Умягчение воды. Как убрать жесткость воды.
- жёсткой называется вода с большим содержанием солей ,
- мягкой с малым содержанием
«Жёсткая» вода — исторически: ткань, постиранная с использованием мыла на основе жирных кислот в жёсткой воде — более жёсткая на ощупь. Этот факт объясняется, с одной стороны, отложением на ткани кальциевых и магниевых солей жирных кислот, образующихся в процессе стирки. С другой стороны, волокна ткани обладают ионообменными свойствами, и, как следствие, свойством сорбировать многовалентные катионы — на молекулярном уровне.
- временная (карбонатная) жёсткость, — обусловлена гидрокарбонатами кальция и магния Са(НСО3)2; Mg(НСО3)2,
- постоянная (некарбонатная) жёсткость — вызванную присутствием других солей, не выделяющихся при кипячении воды: в основном, сульфатов и хлоридов Са и Mg (CaSO4, CaCl2, MgSO4, MgCl2).
С 1 января 2014 года в России введен межгосударственный стандарт ГОСТ 31865-2012 «Вода. Единица жесткости». По новому ГОСТу жесткость выражается в градусах жесткости (°Ж). 1 °Ж соответствует концентрации щелочноземельного элемента, численно равной 1/2 его миллимоля на литр (1 °Ж = 1 мг-экв/л). В разных странах использовались (иногда используются до сих пор) различные внесистемные единицы — градусы жёсткости.
Нормы жесткости воды — в 99,99% случаев речь идет о временной жесткости, данные ВСТ:
Сравнение принятных норм жесткости воды в РФ и Европе (Германии), данные Эколайн:
Жесткость воды в некоторых городах мира — данные МВК — неизвестной достоверности 🙂
| Жесткость, °Ж | Кальций, мг/л | Магний, мг/л | |
|---|---|---|---|
| Москва | 2,0-5,5 | 46 | 11 |
| Париж | 5,0-6,0 | 90 | 6 |
| Берлин | 5,0-8,8 | 121 | 12 |
| Нью-Йорк | 0,3-0,4 | 6 | 1 |
| Сидней | 0,2-1,3 | 15 | 4 |
Нормативные требования и рекомендации
- Рекомендации всемирной организации здравоохранения (ВОЗ) для питьевой воды:
- кальций – 20-80 мг/л; магний – 10-30 мг/л. Для жесткости какой-либо рекомендуемой величины не предлагается. Московская питьевая вода по данным показателям соответствует рекомендациям ВОЗ.
- Российские нормативные документы (СанПиН 2.1.4.1074-01 и ГН 2.1.5.1315-03) для питьевой воды регламентируют:
- кальций – норматив не установлен; магний – не более 50 мг/л; жесткость — не более 7°Ж.
- Норматив физиологической полноценности бутилированной воды (СанПиН 2.1.4.1116-02):
- кальций – 25-130 мг/л; магний – 5-65 мг/л; жесткость – 1,5-7°Ж.
- По содержанию кальция и магния бутилированная вода высшей категории официально ничем не лучше воды из-под крана
Перевод единиц и градусов жесткости воды — в 99,99% случаев речь идет о временной жесткости:
Перевод единиц жесткости воды в пересчете по кальцию. Вполне можно пользоваться вне зависимости от реального состава жесткости.| °Ж = 1 мг-экв/л | mmol/L | ppm, mg/L | dGH, °dH | gpg | °e, °Clark | °fH | |
| 1 русский °Ж = 1 мг-экв/л это: | 1 | 0,5 | 50,05 | 2,804 | 2,924 | 3,511 | 5,005 |
|---|---|---|---|---|---|---|---|
| 1 ммоль/л = mmol/L это: | 2 | 1 | 100.1 | 5.608 | 5.847 | 7.022 | 10.01 |
| 1 американский° ppmw = mg/L = American degre: | 0,01998 | 0.009991 | 1 | 0.05603 | 0.05842 | 0.07016 | 0.1 |
| 1 немецкий° dGH, °dH это: | 0,3566 | 0.1783 | 17.85 | 1 | 1.043 | 1.252 | 1.785 |
| 1 американская популярная ед. gpg это: | 0,342 | 0.171 | 17.12 | 0.9591 | 1 | 1.201 | 1.712 |
| 1 английский °e, °Clark это: | 0,2848 | 0.1424 | 14.25 | 0.7986 | 0.8327 | 1 | 1.425 |
| 1 французский °fH это: | 0,1998 | 0.09991 | 10 | 0.5603 | 0.5842 | 0.7016 | 1 |
| Пример: 1 °Ж = 50,05 ppm | |||||||
- американские градусы жесткости воды, внимание тут два пункта:
- gpg = Grains per Gallon: 1 гран (0.0648 г) CaCO3 в 1 американском галлоне (3.785 л) воды. Поделив граммы на литры получаем: 17.12 мг/л СаСО3 — это не «американский градус», но очень употребляемая в штатах величина жесткости воды.
- американский градус = ppmw = mg/L = American degre: 1 часть CaCO3 в 1000000 частей воды 1мг/л CaCO3
- английские градусы жесткости воды = °e = °Clark: 1 гран (0.0648 г) в 1 английском галлоне (4.546) л воды = 14.254 мг/л CaCO3
- французские градусы жесткости воды (°fH or °f) (fh): 1 часть CaCO3 в 100000 частей воды, или 10 мг/л CaCO3
- немецкие градусы жесткости воды = °dH (deutsche Härte = «немецкая жесткость» может быть °dGH (общая жесткость) или °dKH (для карбонатной жёсткости)): 1 часть оксида кальция – СаО в 100000 частей воды, или 0.719 частей оксида магния – MgO в 100000 частей воды, что дает 10 мг/л СаО или 7.194 мг/л MgO
- русский (РФ) градус жесткости воды °Ж = 1 мг-экв/л: соответствует концентрации щелочноземельного элемента, численно равной 1/2 его миллимоля на литр, что дает 50,05 мг/л CaCO3 or 20.04 мг/л Ca2+
- ммоль/л = mmol/L: соответствует концентрации щелочноземельного элемента, численно равной 100.09 мг/л CaCO3 or 40.08 мг/л Ca2+
Методы устранения жесткости воды
- Термоумягчение. Основан на кипячении воды, в результате термически нестойкие гидрокарбонаты кальция и магния разлагаются с образованием накипи:
- Ca(HCO3)2 → CaCO3↓ + CO2 + H2O.
- Кипячение устраняет только временную (карбонатную) жёсткость. Находит применение в быту.
- Реагентное умягчение. Метод основан на добавлении в воду кальцинированной соды Na2CO3 или гашёной извести Ca(OH)2. При этом соли кальция и магния переходят в нерастворимые соединения и, как следствие, выпадают в осадок. Например, добавление гашёной извести приводит к переводу солей кальция в нерастворимый карбонат:
- Ca(HCO3)2 + Ca(OH)2 → 2CaCO3↓ + 2H2O
- Лучшим реагентом для устранения общей жесткости воды является ортофосфат натрия Na3PO4, входящий в состав большинства препаратов бытового и промышленного назначения:
- 3Ca(HCO3)2 + 2Na3PO4 → Ca3(PO4)2↓ + 6NaHCO3
- 3MgSO4 + 2Na3PO4 → Mg3(PO4)2↓ + 3Na2SO4
- Ортофосфаты кальция и магния очень плохо растворимы в воде, поэтому легко отделяются механическим фильтрованием. Этот метод оправдан при относительно больших расходах воды, поскольку связан с решением ряда специфических проблем: фильтрации осадка, точной дозировки реагента.
- Катионирование. Метод основан на использовании ионообменной гранулированной загрузки (чаще всего ионообменные смолы). Такая загрузка при контакте с водой поглощает катионы солей жёсткости (кальций и магний, железо и марганец). Взамен, в зависимости от ионной формы, отдаёт ионы натрия или водорода. Эти методы соответственно называются Na-катионирование и Н-катионирование.
- При правильно подобранной ионообменной загрузке жёсткость воды снижается при одноступенчатом натрий-катионировании до 0,05-0,1 °Ж, при двухступенчатом — до 0,01 °Ж.
- В промышленности с помощью ионообменных фильтров заменяют ионы кальция и магния на ионы натрия и калия, получая мягкую воду.
- Обратный осмос. Метод основан на прохождении воды через полупроницаемые мембраны (как правило, полиамидные). Вместе с солями жёсткости удаляется и большинство других солей. Эффективность очистки может достигать 99,9 %.
- Различают нанофильтрацию (условный диаметр отверстий мембраны равен единицам нанометров) и пикофильтрацию (условный диаметр отверстий мембраны равен единицам пикометров).
- В качестве недостатков данного метода следует отметить:
- — необходимость предварительной подготовки воды, подаваемой на обратноосмотическую мембрану;
- — относительно высокая стоимость 1 л получаемой воды (дорогое оборудование, дорогие мембраны);
- — низкую минерализацию получаемой воды (особенно при пикофильтрации). Вода становится практически дистиллированной.
- Электродиализ. Основан на удалении из воды солей под действием электрического поля. Удаление ионов растворенных веществ происходит за счёт специальных мембран. Так же как и при использовании технологии обратного осмоса, происходит удаление и других солей, помимо ионов жёсткости.
Источник
Что такое жесткость воды и как ее определить
Жесткость воды — это содержание солей, которое зависит от состава, физико-химических свойств, численного количества примесей. Превышение этого показателя одинаково вредно для питьевых, бытовых и технических жидкостей. При доставке горячих, холодных, производственных водных растворов потребителям поставщики обязаны соблюдать нормированные параметры, установленные законодательством. Частные лица, берущие водичку из личных колодцев, должны самостоятельно заботиться о её качестве. Читайте далее, что такое жесткость воды, как ее определить, чем она измеряется, как привести жидкость в нормальное состояние для безопасного использования.
Жесткость в питьевой воде
Под термином жесткость воды понимается количество растворенных и нерастворенных солей, присутствующих в природных водных залежах. Водица может быть слишком мягкой или слишком жесткой. Вредны оба варианта. Недостаток солей нарушает водно-щелочной баланс в организме, избыток вызывает множественные заболевания важных органов: сердца, почек, кожи, печени. При переизбытке солей жидкость имеет горьковато-металлический вкус, может быть мутной, с разными цветовыми оттенками.
Соблюдение нормы жесткости питьевой воды очень важно для потребителей. Солями можно отравиться, они вызывают расстройство желудка, пожелтение кожи, иные неприятности. Высокая концентрация солей жесткости отрицательно сказывается на работе бытовых приборов — примеси образуют трудно-очищающуюся накипь, каменистые известковые отложения. Из-за них образуются шлаки в системе водоснабжения, быстро выходят из строя бытовые/промышленные приборы, сантехника, гидрооборудование.
Какие соли обуславливают жесткость природной воды, откуда они берутся
Основные соли жесткости, присутствующие в воде — это разные соединения:
- нитраты, хлориды, карбонаты магния;
- бикарбонаты, сульфаты, сульфиды кальция.
После естественного испарения или после принудительного выпаривания водного раствора соли становятся видимыми, остаются в сосуде. Именно они образуют отложения на дне и стенках посуды, чайников, санприборов. По жесткости воды легко определить, какая соль в ней явственнее присутствует. Примеси магния труднее растворяются, придают напиткам вкус горечи.
От чего зависит присутствие соли жесткости в воде
Степень жёсткости для питьевой воды определяется типом и количеством водных солей. В разной местности показатели различные. Соли проникают в водоносные пласты, вымываясь из залежей горных пород: известняков, гипсов, доломитов.
Показатели жёсткости воды являются величинами переменными, они зависят от разных факторов:
- процессов, происходящих в земной коре;
- пластов залежей ископаемых, через которые проходят водные потоки;
- интенсивности растворения песчано-каменистых пород;
- смены сезонов.
У вод, лежащих близко к поверхности и залегающих на глубине, параметры разные. Они выше там, где водный поток проходит через слои известняков. Весной, при обилии талых потоков, при их попадании в водоемы и при просачивании в подземные водные пласты, количество солей снижается. Зимой концентрация выше.
Классификация воды с солями жесткости
Какие соли жесткости присутствуют в воде? Различают общую, постоянную и временную жёсткость:
- Карбонатная (временная) Жк — щелочной раствор с рН>8.3 содержит бикарбонаты, которые при нагревании выпадают в осадок, образуя накипь.
- Некарбонатная (постоянная) Жнк — характеризуется присутствием анионов (хлоридов, нитратов, сульфатов), которые сохраняются даже при кипячении жидкости.
- Общая Жо — это суммированная концентрация присутствия магния и кальция в виде ионных соединений. Сумма получается от сложения временной и постоянной величин: Жо=Жк+Жнк.
При очистке принимаются во внимание все типы: Жо, Жк, Жнк. Предельно допустимая концентрация питьевой воды по жесткости (кратко: ПДК) обычно устанавливается для общей Жо.
Нормы жесткости для воды
Нормирование определяется документами стандартизации: ГОСТ, СанПиН, ТУ. Точные данные получают, проводя испытания проб в аккредитованных лабораториях, в санэпидстанциях. Для фиксирования лабораторных показаний приняты международные единицы измерения жесткости воды:
- моль/м 3 — количество молей на кубический метр жидкости;
- мг-экв/л — миллиграмм-эквиваленты на кубический дециметр (на 1 литр);
- °Ж — градус жесткости.
Измеряемая единица жесткости воды 1°Ж равна 1 мг-экв/л и равна 1/2 миллимоля на литр. Допустимые значения для ионов кальция и магния разные: для Ca2+1°Ж=20,04, для Mg2+1°Ж=12,16 мг/л (примечание: эти показатели вставляются в расчетную формулу, см. далее по тексту*).
По структуре вода может быть мягкой, средней, жесткой. Мягкой считается дистиллированная, кипяченая, дождевая, талая водичка. Жидкость средней жёсткости поступает из централизованных водопроводов. Артезианская и родниковая водица тоже отличаются средними показателями. К сильножесткой относится вододобыча из соленых водоемов, нуждающаяся в опреснении. В таблице показаны концентрации солей в разных размерных единицах.
Предельно допустимое содержание солей жесткости в воде
| Степень жесткости воды | Показатель в мг-экв/л | Показатель в °Ж | Показатель в ppm |
| Слишком мягкая | до 1,5 | до 1-1,5 | 0-70 |
| Мягкая | 1,5-4 | 1,6-4 | 71-140 |
| Среднежёсткая | 5-8 | 5-12 | 141-210 |
| Сильножёсткая | 9-12 | 13-22 | 211-320 |
| Сверхжёсткая | свыше 12 | 23-34 | 321-530 |
Нормы жесткости для питьевой воды
В СанПиН указаны вариативные величины, в зависимости от применения водных растворов. Жесткость воды по ГОСТУ также регламентируется в зависимости от типа и назначения жидкостей:
- Для обычной сетевой водицы определяется концентрация магния (до 50 мг/л).
- В бутилированной учитываются показатели Ca = 25-130 и Mg = 5-65 мг/л.
- Для воды, использующейся в хозяйственно-питьевых целях ПДК питьевой воды по жесткости не должно превышать 350 мг/л (7-10 мг-экв/л или 1-1,5 грамма на литр).
- Для напитков высшей категории нормой является Жо=1,5-7, для первой не более 7 мг-экв/л.
- По ВОЗ-нормативам в питьевой водице допустимо 10-30 мг магния и 20-80 мг кальция на 1 литр.
- Общая жесткость для питьевой воды по EC не выше 1,2 мг-экв/л.
Нормативно установлены нижние пределы показателей жесткости питьевой воды. В нормальной водичке обязательно должно присутствовать небольшое количество солей. Кальций полезен для организма, из напитков его микроэлементы усваивается лучше, чем из продуктов. Массовая концентрация кальция в питьевой воде не должна быть ниже 0,12, магния меньше 0,04, сульфатов и хлоридов менее 2 мг/дм 3 . Мягкая водичка вымывает из тела кальций, вызывая неприятные последствия — разрушаются кости и зубы. Слишком жесткая вызывает образование камней в организме, нарушает работу системы выделения. Соленая вода разрушительно действует на оборудование гидросистем, засоряет отложениями стенки трубопроводов, увеличивает расходы на нагрев.
Если в воде солей жесткости больше, чем предписано стандартами, нужно её очистить до допустимых показателей. В табличке указаны степени солевой концентрации по шкале жёсткости с показателями в промилле.
Шкала жесткости
| Концентрация солей | Величина в ppm (в промилле или мг/л) |
| Представляющая опасность для жизни | свыше 500 |
| Предельно допустимая | 500 |
| Средний показатель вод, добываемых из природныхводоемов | 400 |
| Допустимое значение воды, подающейся из водопровода | 300 |
| После прохождения угольных фильтров | 170 |
| После очистки системой обратного осмоса | 0-50 |
Нормы жесткости для технической воды
Какой должна быть жесткость котловой воды — норма устанавливается отдельно для котлов с разным давлением:
- до 1,4 МПа (14 кгс/см 2 ) = 15-20;
- 2,4 МПа (24 кгс/см 2 ) = 10-15;
- 3,9 Мпа (40 кгс/см 2 )= 4-10 мкмоль/дм 3 (мкг-экв/дм 3 ).
Первая (меньшая) цифра указывается для котлов, работающих на жидком топливе при тепловом потоке свыше 350 кВт на кв. метр. Вторая (большая) цифра — для котлов, работающих на иных видах топлива при тепловом потоке до 350 кВт/м 2 .
ГОСТ по определению жесткости в воде подскажет, какие параметры допустимы:
Раздельно нормируется питьевая вода по жесткости разных категорий: дистиллированная, сетевая, разливная. Для солей железа показатели рассчитываются отдельно.
Как определить жесткость воды
Очень сложно определить на ощупь, какая вода — жесткая или мягкая. Термин «жёсткость» возник потому, что после стирки ткани теряют мягкость, шерстистость или шелковистость, становятся неприятно жесткими на ощупь. Ткацкие или трикотажные переплетения, независимо от плотности, имеют пористую структуру. К волокнам присоединяются соли, что делает вещи после стирки более грубыми, жесткими, плотными.
Определить жесткость воды в можно как в лаборатории, так и в домашних условиях. Наличие солей жесткости можно определить визуально:
- Напитки имеют неприятный горчащий вкус.
- Чаи завариваются дольше обычного.
- Мясо при варке становится неприятно жестким.
- На стенках посуды заметны солевые отложения.
- На приборах образуется обильная накипь.
- На волосах после мытья и на расческе остается белесый налет.
- Мыло и порошок плохо пенятся, при стирке увеличивается их расход.
Повышенная жесткость питьевой воды может причинить ущерб здоровью и нагревательным приборам. Не зная точных показателей концентрации солей, сложно рассчитать дозу средств от накипи для стирально-сушильных агрегатов или запрограммировать на чистку кофемашину. Трудно обеспечить комфортное обитание рыбкам в аквариуме или правильно выбрать фильтры очистки. Помимо визуальной оценки лучше использовать более точные измерительные методы определения жесткости питьевой и технической воды.
Измерение жесткости воды
Перед употреблением в пищу, перед поливом огорода, перед подачей в трубопроводы или перед техническим применением воды для производственных процессов полезно проверить наличие солей жесткости. Такая проверка снимет претензии потребителей к водоснабжающим компаниям, продлит срок службы дорогого промышленного оборудования.
Для измерения жесткости воды используют бытовые и профессиональные приборы:
- Медицинские полоски, продающиеся в аптеках, выдают хороший результат с точностью до 1-2°Ж.
- Экспресс-тесты для аквариума позволяют следить за подачей воды в емкости с водными обитателями или проверять растворы, предназначенные для полива растений.
- Солемер, спектроанализатор, TDS и EC-метр показывают содержание солей и иные параметры: удельную электропроводность, сопротивление раствора.
Полезно заказать исследование в лаборатории, чтобы получить точные результаты с подтверждающей документацией. Тогда не придется думать, чем определить жесткость воды, не нужно покупать измерительные приборы или рассчитывать показатели по косвенным параметрам, используя формулы.
Как определить жесткость воды по формуле
Определить жесткость воды можно по формуле. Для определения общих показателей нужно выполнить расчет:
Жо = [Ca 2+ ] + [Mg 2+ ] = (m(Ca 2+ ))/(Э(Ca 2+ ) x V(H2O)) + (m(Mg 2+ ))/(Э(Mg 2+ ) x V(H2O)),
[Ca 2+ ]; [Mg 2+ ] — концентрация ионов кальция и магния, в мг-экв/дм3;
m(Ca 2+ ); m(Mg 2+ ) — содержание ионов в мг;
V(H2O) — объем воды, дм 3 ;
Э -эквивалентная масса ионов* (её значения уже приводились в тексте: Ca 2+ =20,04; Mg 2+ =12,16 мг/лили г/моль).
Расчетный результат получается в единицах: мг-экв/дм 3 .
Далее вычисляют временную или постоянную жёсткость. Рассчитанную величину вычитают из Жо и получают значения всех трёх категорий Ж.
Карбонатная Жк вычисляется по формуле:
Как понизить жесткость в питьевой воде
Понизить жесткость питьевой воды можно бытовыми способами и с помощью профессионального оборудования. Для умягчения водных составов в быту применяют простые и доступные методы: кипячение, отстаивание, заморозка с оттаиванием. Используют дистилляты и бытовые фильтры.
Длительным кипячением (20-30 минут) можно устранить карбонатную жёсткость — гидрокарбонаты разлагаются, выделяя углекислый газ и отложения накипи:
Ca 2+ +2HCO3-=CaCO3↓+H2O+CO2↑(стрелками показаны: ↓ — осадок, ↑ — улетучивание);
Для загородных домов и промышленного умягчения используют профессиональные установки солеочистки:
- Фильтры умягчения, их работа основана на натрий-катионировании — замещении ионов присутствующих солей катионами натрия.
- Ионообменные фильтры с многокомпонентными смолами (Экотар, Экомикс) сразу производят обессоливание и обезжелезивание.
- Обратный осмос — лучший вариант очистки с помощью мембран. При его использовании обеспечена допустимая норма жесткости воды без прочих дополнительных систем фильтрации.
На сайте компании Diasel можно купить любые фильтры для удаления из воды солей жесткости. Мы продаем комплектующие к установкам обратного осмоса, соберем для вас комплексные линии очистки, предоставим реагенты для снижения уровня безопасности основного жизненного напитка. Гарантируем консультации по любым вопросам, помощь по монтажным работам, текущему и сервисному обслуживанию. С нашими профессиональными установками жесткость воды всегда будет в норме.
Источник