- Способы разделения смесей
- Разделение смеси методом отстаивания
- Разделение смеси мела и воды фильтрованием
- Разделение смеси поваренной соли и воды выпариванием
- Разделение смеси газов
- Заключение
- Вода с солью как разделить
- Способы разделения смесей
- Отстаивание
- Центрифугирование
- Фильтрование
- Действие магнитом
- Выпаривание. Кристаллизация
- Дистилляция (перегонка)
- Очистка воды от соли
- Какие соли в воде нужно очистить
- Что будет, если много соли в воде
- Как вода с повышенным содержанием солей влияет на организм
- Как вода с высоким содержанием соли воздействует на оборудование
- Нормы солености воды
- Вода с высоким содержанием соли — как определить количество солей в воде
- Как очистить воду от соли
- Обратный осмос — основной метод очистки воды от солей
- Польза обратноосмотических установок обессоливания
Способы разделения смесей
Как мы уже знаете, каждое вещество в составе смеси сохраняет свои свойства. Это позволяет разделять смеси на отдельные вещества. Чтобы ознакомиться со способами разделения смесей, выполним опыты.
Разделение смеси методом отстаивания
Приготовим смесь мела и воды. Для этого на дно прозрачной сосуды поместим 1 столовую ложку порошка мела, по стеклянной палочке добавим полстакана воды и перемешаем. Образуется смесь белого цвета, которая, постояв несколько минут, разделится на два слоя. Слой мела осядет на дно, а слой воды будет находиться над ним. Такое происходит потому что мел в воде не растворяется и он тяжелее воды. Осторожно слив воду, мы разделим эту смесь. Такой способ разделения смесей получил название отстаивания.
Разделение смеси мела и воды фильтрованием
Однако полностью разделить смесь мела и воды с помощью отстаивания не удается. Как достичь полного разделения смеси этих веществ? Выполним еще один опыт.
Смесь мела и воды пропустим через фильтр — плотный материал из специальной бумаги или ткани. Мы увидим, что вода проникает через фильтр в посуду-приемник, а мел остается на фильтре. Этот способ разделения смесей получил название фильтрования.
Фильтры изготавливаются из специальной бумаги, который так и называется — фильтровальная, или из тканей различной плотности. Фильтром может быть слой чистого песка или ваты. Кстати, в городских водоочистных станциях применяют песчаные фильтры. Толщина слоя песка в них достигает 1 м.
Как видим, отстаиванием и фильтрованием можно разделить смесь воды и нерастворимого в ней вещества.
Разделение смеси поваренной соли и воды выпариванием
Как вы знаете, поваренная соль хорошо растворяется в воде. Такую смесь веществ отстаиванием разделить нельзя. А удастся это сделать фильтрацией? Выполним опыт. Пропустим смесь воды и поваренной соли через бумажный фильтр. Мы увидим, что соли на фильтре не осталось.
Итак, если вещество хорошо растворяется в воде, то отстаивание и фильтрование не подходят для разделения такой смеси. Для этого существует другой способ — выпаривания.
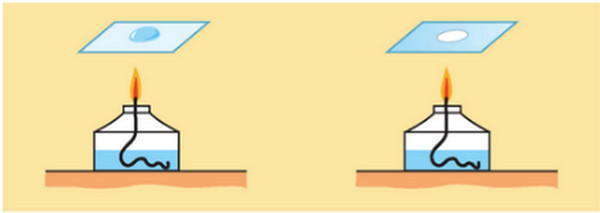
Капните небольшое количество смеси воды и поваренной соли на стекло и начнем нагревать его до тех пор, пока вся вода не испарится. После того как вода испарится, на стекле останется пятно белого цвета. Это и есть поваренная соль. С помощью выпаривания мы разделили смесь воды и поваренной соли.
Разделение смеси газов
Вы уже знаете способы выделения составных частей из смеси твердых и жидких веществ. А как разделить смесь газообразных веществ? Рассмотрим это на примере воздуха.
Итак, азот и кислород, которых больше всего в составе воздуха, схожи по физическим свойствам. Они плохо растворяются в воде, не имеют цвета и запаха. Оба газа образуют столь однородную смесь, что отстаиванием или фильтрацией их нельзя разделить. Поэтому азот и кислород выделяют из воздуха с помощью выпаривания. Сначала воздух переводят в жидкое состояние, охлаждая его до очень низкой температуры (около -200 ° С), а затем подвергают выпариванию. Первым испаряется азот, а после него — кислород. Каждый газ собирают в баллоны отдельно и используют по назначению.
Заключение
Разделение смеси — это выделение из нее чистых веществ.
Чтобы разделить смесь, необходимо знать свойства веществ, которые входят в ее состав.
Теперь вы знаете, что существуют различные способы разделения смесей: отстаивание, фильтрование, выпаривание.
Источник
Вода с солью как разделить
16 лет успешной работы в сфере подготовки к ЕГЭ и ОГЭ!
1602 поступивших (100%) в лучшие вузы Москвы
Подготовка к ЕГЭ, ОГЭ и предметным Олимпиадам в Москве
- home
- map
У Вас возникли вопросы?
Мы обязательно Вам перезвоним:
Видео с опытом по выпариванию соли демонстрирует один из самых простых способов разделения смесей веществ. Изучайте химию вместе с нами!
Преобладающее количество веществ нашей планеты находятся в виде соединений, смесей и растворов, а не в чистом виде. Существует множество способов получения чистых веществ, как в химических лабораториях, так и в промышленности и быту. Способов разделения смесей существует несколько: фильтрование (отделение нерастворимых веществ), выпаривание соли и других растворимых веществ, дистилляция и др.
Метод выпаривания применяют для того, чтобы сделать раствор более концентрированным, для того, чтобы выделить растворенные в растворе вещества или для того, чтобы получить растворитель в чистом виде.
В основном выпаривают водные растворы, растворы нелетучих или малолетучих веществ.
В лабораторных условиях выпаривание соли (видео) производят следующим образом. Сначала растворяют поваренную соль в воде. Фильтруют ее от примесей. Помещают сосуд над горелкой и греют до тех пор, пока вся вода не испарится, и на дне не будет сухая соль в виде кристаллов.
В промышленных условиях для выпаривания соли применяют специальные выпарные аппараты и установки.
Издревле выпаривали соль из морской воды путем естественного испарения. Морская вода собиралась в специальных водоемах и за несколько лет вода испарялась и соль кристаллизовалась.
Источник
Способы разделения смесей
Для получения чистых веществ используют различные способы разделения смесей.
| Способы разделения смесей | |
|---|---|
| неоднородных (гетерогенных) | однородных (гомогенных) |
| — Отстаивание — Фильтрование — Действие магнитом — Центрифугирование | — Выпаривание. Кристаллизация. — Дистилляция (перегонка) |
Процессы разделения смесей основаны на различных физических свойствах компонентов, образующих смесь.
Отстаивание
Отстаивание — это разделение неоднородной жидкой смеси на компоненты, путём её расслоения с течением времени под действием силы тяжести.
Отстаиванием можно разделить смесь нерастворимых в воде веществ, имеющих разную плотность.
Пример. Смесь из железных и древесных опилок можно разделить, если высыпать её в сосуд с водой (1), взболтать и дать отстояться. Железные опилки опустятся на дно сосуда, а древесные будут плавать на поверхности воды (2), и их вместе с водой можно будет слить в другой сосуд (3):
На этом же принципе основано разделение смесей малорастворимых друг в друге жидкостей.
Пример. Смеси бензина с водой, нефти с водой, растительного масла с водой быстро расслаиваются, поэтому их можно разделить с помощью делительной воронки:
Отстаиванием также можно разделить вещества, которые осаждаются в воде с различной скоростью.
Пример. Смесь из глины и песка можно разделить, если высыпать её в сосуд с водой (1), взболтать и дать отстояться. Песок оседает на дно значительно быстрее глины (2):
Этот способ используется для отделения песка от глины в керамическом производстве (производство глиняной посуды, красных кирпичей и др.).
Центрифугирование
Центрифугирование — это разделение неоднородных жидких смесей путём вращения.
Пример. Если компоненты неоднородной жидкой смеси очень малы, такие смеси разделяют центрифугированием. Такие смеси помещают в пробирки и вращают с большой скоростью в специальных аппаратах — центрифугах.
Перед центрифугированием частицы смеси распределены по объёму пробирки равномерно. После центрифугирования более лёгкие частицы всплывают наверх, а тяжёлые оседают на дно пробирки.
С помощью центрифугирования, к примеру, отделяют сливки от молока.
Фильтрование
Фильтрование — это разделение жидкой неоднородной смеси на компоненты, путём пропускания смеси через пористую поверхность. В роли пористой поверхности может выступать бумажная воронка, марля, сложенная в несколько слоёв, или любой другой пористый материал, способный задержать один или несколько компонентов смеси.
Фильтрованием можно разделить неоднородную смесь, состоящую из растворимых и нерастворимых в воде веществ.
Пример. Чтобы разделить смесь, состоящую из поваренной соли и песка, её можно высыпать в сосуд с водой, взболтать и затем эту смесь пропустить через фильтровальную бумагу. Песок остаётся на фильтровальной бумаге, а прозрачный раствор поваренной соли проходит через фильтр:
При необходимости, растворённую поваренную соль из воды можно выделить выпариванием.
Действие магнитом
С помощью магнита из неоднородной смеси выделяют вещества, способные к намагничиванию.
Пример. C помощью магнита можно разделить смесь, состоящую из порошков железа и серы:
Выпаривание. Кристаллизация
Выпаривание — это способ разделения жидких смесей путём испарения одного из компонентов. Скорость испарения можно регулировать с помощью температуры, давления и площади поверхности испарения.
Пример. Чтобы растворённую в воде поваренную соль выделить из раствора, последний выпаривают:
Вода испаряется, а в фарфоровой чашке остаётся поваренная соль. Иногда применяют упаривание, т. е. частичное испарение воды. В результате образуется более концентрированный раствор, при охлаждении которого растворённое вещество выделяется в виде кристаллов. Этот процесс получил название кристаллизации.
Дистилляция (перегонка)
Дистилляция (перегонка) — это способ разделения жидких однородных смесей путём испарения жидкости с последующим охлаждением и конденсацией её паров. Данный способ основан на различии в температурах кипения компонентов смеси.
Пример. При нагревании жидкой однородной смеси сначала закипает вещество с наиболее низкой температурой кипения. Образующиеся пары конденсируются при охлаждении в другом сосуде. Когда этого вещества уже не останется в смеси, температура начнёт повышаться, и со временем закипает другой жидкий компонент:
Таким способом получают, к примеру, дистиллированную воду.
Источник
Очистка воды от соли
Количество солей — солесодержание — входит в число основных показателей, определяющих качество воды, применяемой для приготовления еды, питья, полива, технических нужд. Соли состоят из металлов, гидроксилов, кислотных остатков. В небольшом количестве их присутствие — минерализация воды — улучшает её вкусовой и химический состав. В избыточном сильно ухудшает, приносит большой вред здоровью человека и природе — почвам, водоемам, флоре, фауне. В водном растворе должны присутствовать соли в количестве, предписанном стандартами. Процесс очистка воды с солью до нормально допустимого состояния называется обессоливанием (деминерализацией).
Какие соли в воде нужно очистить
К солям относятся соединения металлов с разными химическими веществами. В зависимости от состава они делятся на несколько групп.
| Группа | Содержание других веществ, помимо металлов | Название соли, формула | |||||||||||||
| Соленость | Минерализованность |
| Ультрапресная — менее 100 мг/л | Пресная — до 1 г/л |
| Пресная — до 1000 мг/л | Слабоминерализованная — 1-2 г/л |
| Слабопресная — 1001-3000 мг/л | Малой минерализации — 2-5 г/л |
| Соленая — 3001-10000 мг/л | Среднеминерализованная — 5-15 г/л |
| Сильносоленая — 10001-50000 мг/л | С высокой минерализацией — 15-30 г/л |
| Рассол — 50000-300000 мг/л | Рассольные минводы — 35-150 г/л |
| Ультрарассол — выше 300000 мг/л | Крепкорассольные — более 150 г/л |
Наиболее полезна для организма пресная, слабоминерализованная вода с солевой концентрацией 100 мг/л (100 ppm). Предел общей минерализации ПДК = 1000 мг/л, вкусной считается жидкость с солесодержанием 500–600 мг/литр. Предельно допустимое количество хлоридно-сульфатных соединений — 200–400, гидрокарбонатных — 250–500, фосфатных — 3,5 мг/л.
Строгие нормы солесодержания устанавливают в промышленности для рабочей технической жидкости. Для ТЭЦ и ТЭС численность солей не должна превышать 30–100 мкг-экв/кг. Даже морскую воду можно очистить от растворенных в ней солей с помощью фильтрования и затем использовать для любых целей.
Вода с высоким содержанием соли — как определить количество солей в воде
Присутствие солевых примесей ощущается органолептически:
- Вкус солоноватый, с неприятной кислотной горчинкой или горько-соленый.
- Запах с резковатым характерным оттенком.
- Сероватый или белёсый налет на посуде.
- Длительная варка овощей, жесткость вареного мяса.
- Стянутость кожи, покалывание после мытья.
- Сухость, ломкость волос.
- В жесткой воде слабее проявляются пенящие свойства моющих средств, возрастает их расход.
Точное количество солевых примесей можно определить, заказав химический анализ в лаборатории. Там вычислят общую минерализацию, численность отдельных веществ, сухой остаток. На основе полученных расчетов легко выбрать промышленные и бытовые установки по очистке воды от солей.
Значения ПДК для некоторых элементов в мг/л:
- натрий — 200;
- кальций — 100;
- магний — 50;
- калий — 12;
- медь — 1,0;
- железо — 0,3.
Можно самостоятельно выполнить измерения с помощью специальных переносных приборов — солемеров. Анализатор TDS-метр меряет общее количество веществ в водном растворе (численность солесодержащих частиц на 1 миллион частичек воды: 1 ppm = 1 мг/л) и выдает показатель минерализации, зависящий от суммарной концентрации ионов (положительных катионов, отрицательных анионов).
Солесодержание зависит от температуры. При нагреве воды отложения на дне и стенках посуды намного интенсивнее, чем в сосудах с холодной водой. При разной температуре измерения будут отличаться. При выборе установок для очистки воды с солью ориентируются на усредненные годовые показатели. Чтобы их получить, нужно сдавать пробы на анализ каждый сезон.
Как очистить воду от соли
Как можно удалить соль из воды — очистку производят разными способами. Бытовую воду, текущую из крана, можно отстаивать, дистиллировать, заморозить/разморозить, профильтровать или прокипятить. Эти способы подходят для обработки небольшого количества водных растворов.
Жидкость, добытую из природных открытых или глубинных подземных источников, обрабатывают более тщательно сложными промышленными способами, среди которых применяются:
- Механическая очистка от примесей, присутствующих в виде крупных частиц величиной от 5 мкм.
- Очистка с помощью разнообразных осадочных фильтров, которые улавливают мелкие частицы.
- Использование химических реагентов — смол, извести, сульфаугля.
- Электродеионизация с помощью ионообменного материала.
- Обратный осмос — особо эффективный мембранный вариант обессоливания.
При выборе способы очистки воды от солей, при подборе оборудования учитываются: производственные задачи, назначение жидкости, мощность подачи потока, давление, прочие факторы.
Обратный осмос — основной метод очистки воды от солей
При обратносмотическом процессе водный раствор пропускается через микроскопические капилляры мембраны. Через них молекулы воды проникают беспрепятственно, но задерживаются все остальные микрочастицы. Можно ли очистить воду от соли на 99,9 % — установки, которые продаются на сайте компании Diasel, очень глубоко производят удаление всех солей и примесей. Показатель качества очистки воды от солей и металлов близок к 100 %.
Компактная линия, с помощью которой легко убрать соли воды, выполняет сразу несколько функций. Помимо солей она удаляет другие вредоносные примеси, производя комплексную очистку от нежелательных химических веществ. Процесс не образует отложений, которые могут засорить систему или проскользнуть в очищенный раствор. Жидкость становится прозрачной, мягкой, пригодной для разных нужд — для мытья, еды и питья, для подачи в бытовую технику и промышленные системы.
На сайте компании «Диасел» можно купить разные обратноосмотические системы очистки воды от солей:
- Установки обратного осмоса для различных промышленных предприятий.
- Двухступенчатые установки различной производительностью от 50 литров до 20 м 3 /час используют в медицине, в энергетике, радиоэлектронике, металлургии.
- Установки на весь дом востребованы в частном домостроении. Их приобретают владельцы загородных особняков, дачных коттеджей, подводящие воду из автономных источников.
- Бытовые системы обратного осмоса пользуются спросом даже у владельцев небольших предприятий общественного питания. В доме компактное устройство размещается под кухонной раковиной и обеспечивает жильцов полезной деминерализованной водицей.
Установки, производящие удаление солей воды, извлекают до 98-99 % примесей, качественно улучшая вкус воды.
Польза обратноосмотических установок обессоливания
Вода, подвергнутая очистке, при нагревании не образует накипь. Надолго продлевается срок службы промышленной техники, бытовых приборов, всех систем жизнеобеспечения — отопительных, водопроводных, канализационных. Очищенные водные растворы можно безопасно использовать на производстве, в гидротехнических сооружениях, в котельных станциях.
Затраты на приобретение установки обратного осмоса быстро окупятся, принесут пользу. Избавят от протечек, поломок гидрооборудования, проблем со здоровьем.
Купить обратный осмос, способный очистить воду от растворенных солей, от взвешенных примесей и коллоидных частиц, удобно в Diasel Engineering. Инженеры компании подберут комплекс, соответствующий задачам частных клиентов, общественных организаций, промышленных производств. Выполнят установку, запуск, тестирование. Дадут исчерпывающую консультацию по использованию оборудования. Обеспечат гарантийное и текущее обслуживание.
Источник