Биологическая роль гидролиза в процессах жизнедеятельности организма

Продукты полного гидролиза углеводов – глюкоза, галактоза и фруктоза – через клетки кишечника поступают в кровь.

В 12-перстную кишку поступает желчь и сок поджелудочной железы, необходимые для переваривания жиров. В соке поджелудочной железы содержится фермент липаза, катализирующий гидролиз сложноэфирной связи в триацилглицеринах. Поскольку жиры нерастворимы в водных средах, а липаза нерастворима в жирах, гидролиз происходит лишь на поверхности раздела этих фаз и, следовательно, скорость переваривания зависит от площади этой поверхности.
В составе желчи содержатся коньюгированные желчные кислоты (Рис.5) – гликохолевая и таурохолевая. Эти кислоты обладают амфифильными свойствами. На поверхности раздела жир-вода они ориентируются таким образом, что гидрофобная циклическая часть оказывается погружённой в жир, а гидрофильная боковая цепь – в водную фазу. В результате образуется стабильная эмульсия.

Образующиеся в процессе переваривания пищи вещества-мономеры, вступают в ряд реакций. Во многих из них они окисляются, и энергия, выделяющаяся при этом окислении, используется для синтеза АТФ из АДФ – основного процесса аккумулирования энергии в живых организмах. Эта энергия необходима для роста и нормального функционирования организма. Человек получает её как за счёт многостадийного процесса окисления пищи – белков, жиров и углеводов, так и за счёт гидролиза некоторых сложных эфиров, амидов, пептидов и гликозидоа. Однако главным источником энергии для многих биологических процессов – биосинтеза белка, ионного траспорта, сокращения мышц, электрической активности нервных клеток – является аденозинтрифосфат (АТФ).
АТФ (Аденозинтрифосфорная кислота)
принадлежит к бионеорганическим соединениям, так как состоит из органической части – аденозина и неорганической части – трёх связанных в цепь фосфатных групп. При рН ³ 7,0 АТФ существует в виде аниона АТФ 4- , так как все фосфатные группы при этом значении водородного показателя ионизированы.
Гидролиз АТФ записывают в виде кислотно-основного равновесия::
АТФ 4- + Н2О Û АДФ 3- + НРО4 2- + Н+
DGо = -30,5 кДж/моль,
где АДФ 3- — анион аденозидифосфата.
Как видно, гидролиз соповождается убылью энергии Гиббса
(DGо = -30,5 кДж/моль). Гидролиз может идти и дальше до образования аденозинмонофосфата (АМФ) и, наконец, до аденозина.

В химической формуле они традиционно обозначаются знаком
(тильда). В молекуле АДФ только одна высокоэнергетическая связь; в результате синтеза АТФ путём окилительного фосфорилирования добавляется ещё одна, т.е. энергия окисления субстрата трансформируется в энергию химических связей в молекуле АТФ.
Источник
Вода содержит две макроэнергетические связи
Подробное решение параграф § 7 по биологии для учащихся 10 класса, авторов Пасечник В.В., Каменский А.А., Рубцов A.M. Углубленный уровень 2019
Вопрос 1. Какие вещества называют неорганическими?
Неорганические вещества — простые вещества и соединения, не являющиеся органическими, т. е. не содержащие углерода, а также некоторые углеродосодержащие соединения (карбиды, цианиды, карбонаты, оксиды углерода и некоторые другие вещества, которые традиционно относят к неорганическим).
Вопрос 2. Какие известные вам организмы содержат много воды?
Алоэ, кактусы, водоросли, медуза, в плодах огурцов и др.
Вопрос 3. Какие неорганические вещества мы употребляем в пищу? Почему?
Воду, минеральные вещества (кальций, магний, йод, фосфор, медь и др.). Они способствуют проникновению веществ в клетки организма, протекание ферментативных и пластических процессов, участвуют в формировании и построении тканей, поддерживают осмотическое давление крови, активируют проведение возбуждения и импульсов, способствуют свертыванию крови и т. д.
Вопрос 4. Какие неорганические вещества содержатся в живых организмах?
Вода, соли минеральных кислот и соответствующие катионы и анионы.
Вопрос 5. Что определяет уникальные физические и химические свойства воды, столь важные для существования живой материи?
Уникальные физические и химические свойства воды определяются особенностями структуры её молекулы, которые возникают в результате специфического расположения электронов в атомах кислорода и водорода.
Вопрос 6. Какие химические связи называют водородными?
Водородные связи — это такие связи, которые возникают между положительно заряженным атомом водорода одной молекулы и отрицательно заряженным атомом другой молекулы.
Вопрос 7. Какие физико — химические свойства воды наиболее важны для обеспечения жизнедеятельности клеток и многоклеточных организмов в разных условиях?
Высокая теплоёмкость (способность поглощать тепло при незначительном изменении собственной температуры) воды предохраняет клетку от резких температурных колебаний, а высокая теплопроводность обеспечивает возможность равномерного распределения теплоты между отдельными частями организма. Высокая теплота испарения используется живыми организмами для предохранения от перегрева: испарение жидкости растениями и животными охлаждает организм и является защитной реакцией на повышение температуры. Вода практически несжимаема, благодаря чему клетки поддерживают свою форму и обладают упругостью. Очень важно, что лёд легче воды, так как вода имеет максимальную плотность при +4°С, поэтому пресные водоёмы не промерзают до дна.
Для живых организмов весьма важно ещё и то, что молекулы воды являются диполями. Дипольный характер молекулы воды определяет её способность ориентироваться в электрическом поле. Именно это свойство воды определяет её уникальность как растворителя.
Вопрос 8. В каких растворителях могут растворяться гидрофобные вещества, а в каких — гидрофильные? Какие растворители вам известны?
Гидрофильные вещества легко разрушается в воде, гидрофобные — в бензине или в бензоле.
Вопрос 9. Используя интернет — ресурсы и другие источники информации, найдите сведения о значении для организма следующих элементов: В, Р, S, Са, Мn, Fe, Со, Zn, Сu. Ответ оформите в виде таблицы.
Вопрос 10. Прочитайте статью «Сахар против льда» и на основе анализа полученной информации предложите свои способы борьбы с гололёдом на дорогах.
При повышении безопасности дорожного движения в снежное время года, мы не должны забывать об экологической обстановке.
Сахар — это интересно, экологично, но скорее всего дорого.
Учитывая все недостатки при использовании соли и солевых растворов, связанных с их негативным воздействием на окружающую среду, наиболее целесообразным является способ предупреждения образования гололеда за счет создания покрытий автомобильных дорог, обладающих противо — гололедными свойствами, что делает возможным механическое удаление снежно — ледяных отложений снегоуборочной техникой и исключения отрицательного воздействия химических реагентов на окружающую среду.
1. К одному из способов образования антигололедных покрытий, разработанному в Словакии, относится «Соленый бетон». Антигололедная добавка с рабочим названием «Соленый бетон» представляет собой обработанные кристаллы против гололедного вещества (NaCl), введенные в минеральную часть асфальтобетона. Минеральная оболочка соли (NaCl) формируется из цемента, мелкозернистого известнякового порошка и дробленого песка. Введение добавки в количестве около 10 % по массе минерального материала является достаточным для достижения желаемого эффекта. При температуре около — 4°С небольшое количество соли (приблизительно 1 %) расплавляет тонкие слои снега. При температуре более низкой (ниже — 4°С) плотность льда нарушается; лед ломается и удаляется с поверхности дороги под действием колес транспортных средств. Если температура особенно низкая ( — 10°С), эффект «Соленого бетона» снижается, но сохраняется возможность достаточно простой очистки поверхности дороги с использованием дорожной щетки и отвала.
2. В Уральском государственном лесотехническом университете (УГЛТУ) для повышения противогололедных свойств асфальтобетона разработан кремнийорганический модификатор МПА — 130, не содержащий хлоридов. Устройство верхнего антигололедного слоя дорожного покрытия на основе гидрофобизирующего модификатора, не содержащего хлоридов, на автомобильных дорогах позволит вести активную борьбу с гололедом, благодаря чему повысится коэффициент сцепления колес автомобилей с дорожным покрытием и будет обеспечена нормальная работа транспорта. Кроме того, применение таких покрытий позволит улучшить экологическую обстановку придорожной полосы за счет отказа от применения хлоридов.
Вопрос 11. Уникальные свойства воды определяются в том числе существованием между её молекулами водородных связей. Возможно ли существование таких связей между молекулами других веществ?
Механизм возникновения водородной связи — частично электростатический и частично донорно — акцепторный.
Характерной чертой водородной связи является расстояние между атомом водорода и другим атомом, её образующим. Оно должно быть меньше, чем сумма радиусов этих атомов.
Межмолекулярная водородная связь образуется между молекулами веществ, в состав которых входят водород и сильно электроотрицательный элемент — фтор, кислород, азот, хлор, сера. Сильно смещенная общая электронная пара от водорода к атому отрицательно заряженного элемента, при этом положительный заряд водорода сконцентрирован в малом объеме, приводит взаимодействие протона с неподеленной электронной парой другого атома или иона, обобществляя её.
Водородную связь обозначают точками, указывая, что она намного слабее ковалентной связи (примерно в 15 — 20 раз).
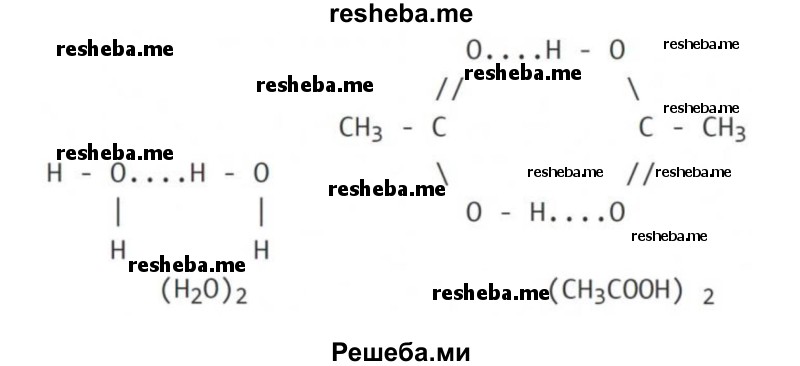
Межмолекулярная водородная связь: две молекулы воды и две молекулы уксусной кислоты с образованием циклической структуры
Вопрос 12. Что произойдёт с клеткой, если концентрации ионов К+, Na+ и Са2+ выровняются и будут одинаковыми как вне, так и внутри её?
От концентрации солей внутри и снаружи клетки зависят буферные свойства цитоплазмы клетки. Буферностью называют способность клетки сохранять определенную концентрацию водородных ионов (рН). В клетке поддерживается слабощелочная реакция (рН 7,2). Пока клетка жива, эти различия в концентрации К+ и Na+ между клеткой и межклеточной средой стойко удерживаются. Если концентрации ионов К+, Na+ и Са2+ выровняются и будут одинаковыми как вне, так и внутри её, клетка просто умрет.
Вопрос 13. Используя доступные информационные источники, уточните, какие условия проведения эксперимента в естественных науках (давление, температура и др.) считаются нормальными. Обсудите с учителем и одноклассниками, почему при нормальных условиях вода (Н20) — это жидкость, а сероводород (H2S) — газ.
Нормальные условия — стандартные физические условия, с которыми обычно соотносят свойства веществ (при нормальных условиях, при н. у., англ. Standard temperature and pressure, STP). Нормальные условия определены IUPAC (Международным союзом чистой и прикладной химии) следующим образом:
Атмосферное давление 101325 Па = 760 мм рт. ст.
Температура воздуха 273,15 K = 0° C.
При нормальных условиях объём 1 моля идеального газа составляет 22,413 996(39) дм³ (молярный объём идеального газа), а количество молекул в 1 см³ составляет 2,686 7774(47)×1019 (постоянная Лошмидта).
Также в справочниках в качестве стандартных условий может указываться температура 298 K, либо +25 °С (298,15 К). Однако такая температура не установлена IUPAC в качестве стандартной, поэтому при использовании справочных данных всякий раз необходимо уточнять, при каких значениях приводятся величины.
Например, Национальный институт стандартов и технологий США (англ. National Institute of Standards and Technology, NIST) использует температуру +20 °C (293,15 K) и давление 101 325 Па (1 атм).
Вода (Н20) — это жидкость, а сероводород (H2S) — газ. Электроотрицательность кислорода выше, чем серы, электронная плотность в молекуле воды более смещена от водорода к кислороду, чем от водорода к сере, в молекуле сероводорода. Молекулы воды образуют между собой прочные водородные связи. В сероводороде водородные связи очень слабые. Поэтому вода при комнатной температуре жидкость, а сероводород — газ.
Или такой ответ, сформулированный иначе: кислород более электроотрицательный элемент, чем сера. Поэтому между молекулами воды возникают более прочные водородные связи, чем между молекулами сероводорода, разрыв этих связей, необходимый для перехода воды в газообразное состояние, требует значительной затраты энергии, что и приводит к аномальному повышению температуры кипения воды.
Источник
Биологическая роль гидролиза в процессах жизнедеятельности организма. АТФ.
Биологическая роль гидролиза в процессах жизнедеятельности организма
Преподаватель: Доцент Русняк Ю.И.
29.11.2004
Биологическая роль гидролиза в процессах жизнедеятельности организма. АТФ.
Гидролиз (греч. hydor вода + lysis разложение) – разложение веществ, проходящее с обязательным участием воды и протекающее по схеме:
AB + H-OH → AH + BOH
Реакции гидролиза подвергаются самые различные вещества. Так в процессе пищеварения высокомолекулярные вещества (белки, жиры, полисахариды и др.) подвергаются ферментативному гидролизу с образованием низкомолекулярных соединений (соответственно, аминокислот, жирных кислот и глицерина, глюкозы и др.).
Без этого процесса не было бы возможным усвоение пищевых продуктов, так как высасываться в кишечнике способны только относительно небольшие молекулы. Так, например, усвоение полисахаридов и дисахаридов становится возможным лишь после полного их гидролиза ферментами до моносахаридов. Точно так же белки и липиды гидролизуются до веществ, которые лишь потом могут усваиваться. Рассмотрим основные реакции гидролиза, протекающие в организме.

Каждый вид организма, каждый орган и каждая ткань содержат свои характерные белки, и при усвоении чужеродных белков пищи организм прежде всего лишает их видовой специфичности. Перед тем, как быть усвоенными белки должны быть разложены на индифферентный материал. Разложение белковых веществ на более простые, лишенные видовой специфичности соединения, способные всасываться в кровь через стенки кишечника, осуществляется в пищеварительных органов человека и животных путем последовательного гидролиза под действием ряда ферментов.
В полости рта белки никаким изменениям не подвергаются, так как в состав слюны необходимые для этого протеолитические ферменты не входят. Переваривание белков начинается в желудке.
В желудочно-кишечном тракте пищевые белки распадаются на аминокислоты при участи пищеварительных протеолитических ферментов – пептидогидролаз. Эта группа ферментов различающихся по субстратной специфичности: каждый из этих ферментов предпочтительно (т.е. с наибольшей скоростью) гидролизует пептидные связи (рис.1), образованные определёнными аминокислотами. В результате совместного действия всех пищеварительных пептидогидролаз белки пищи полностью распадаются на аминокислоты. Таким путём организм получает мономеры для синтеза собственных белков.
В желудке переваривание (т. е. гидролитическое расщепление) происходит при действии протеолитического фермента пепсина; существенную роль в этом процессе играет соляная кислота, за счёт которой желудочный сок имеет низкое значение pH (1-2). Под действием этой кислоты выделяемый главными клетками желудочных желез белок пепсиноген превращается в пепсин. HCl катализирует этот процесс, в ходе которого отщепляется часть молекулы и образуется активный центр фермента. Сам пепсин катализирует процесс своего образования, т. е. является автокатализатором.
Пепсин гидролизирует пептидные связи, удалённые от концов пептидной цепи (поэтому пепсин относят к эндопептидазам). При этом белки распадаются на полипептиды, свободные аминокислоты практически не образуются.
Переваривание белков завершается в верхнем отделе тонкого кишечника под действием ферментов поджелудочной железы и клеток кишечника. Эти клетки продуцируют ряд проферментов (трипсиноген, химотрипсиноген, прокарбопептидазы А и В, проэластаза). После каталитического образования в проферментах активного центра и отщепления части молекул, эти белки превращаются соответственно в ферменты: Трипсин, Химотрипсин, Карбопептидазы А и В и Эластазу.

Карбопептидазы – экзопептидазы. Они гидролизуют пептидную связь, образованную концевым аминокислотным остатком. Карбопептидаза А отщепляет преимущественно концевые аминокислоты с гидрофобным радикалом, а карбоксипептидаза В – остатки лизина и аргинина.
Последний этап переваривания происходит при участии ферментов, синтезируемых клетками кишечника – аминопептидаз и дипептидаз. Первые отщепляют концевые аминокислоты от пептидов, вторые гидролизуют дипептиды.
Таким образом, переваривание пищевых белков – суть, последовательность реакций гидролиза, катализирующегося рядом ферментов.
|
|
|
|

|
|

|

Данный процесс катализируется ферментом аргиназой, причём возможен и обратный процесс – синтез аргинина из орнитина (Цикл Кребса-Гензелейта).

Переваривание начинается уже в ротовой полости: в слюне содержится фермент амилаза (α
1,4 – гликозидаза), расщепляющая α
1,4 гликозидные связи. Поскольку пища в ротовой полости пребывает недолго, то крахмал здесь переваривается лишь частично. Основным же местом перваривания крахмала служит тонкий кишечник, куда поступает амилаза в составе сока поджелудочной железы. Амилаза не гидролизует гликозидную связь в дисахаридах, поэтому основным продуктом действия кишечой амилазы является дисахарид мальтоза.

Продукты полного гидролиза углеводов – глюкоза, галактоза и фруктоза – через клетки кишечника поступают в кровь.

В составе желчи содержатся коньюгированные желчные кислоты (Рис.5)– гликохолевая и таурохолевая. Эти кислоты обладают амфифильными свойствами. На поверхности раздела жир-вода они ориентируются таким образом, что гидрофобная циклическая часть оказывается погружённой в жир, а гидрофильная боковая цепь – в водную фазу. В результате образуется стабильная эмульсия.

Под действием липазы идёт гидролиз жиров, в ходе которого жирные кислоты отщепляются от триацилглицерина одна за другой, сначала от α-углеродных атомов, потом – от β-углеродного атома (Рис. 6)
Образующиеся в процессе переваривания пищи вещества-мономеры, вступают в ряд реакций. Во многих из них они окисляются, и энергия, выделяющаяся при этом окислении, используется для синтеза АТФ из АДФ – основного процесса аккумулирования энергии в живых организмах. Эта энергия необходима для роста и нормального функционирования организма. Человек получает её как за счёт многостадийного процесса окисления пищи – белков, жиров и углеводов, так и за счёт гидролиза некоторых сложных эфиров, амидов, пептидов и гликозидоа. Однако главным источником энергии для многих биологических процессов – биосинтеза белка, ионного траспорта, сокращения мышц, электрической активности нервных клеток – является аденозинтрифосфат (АТФ).
АТФ (Аденозинтрифосфорная кислота) принадлежит к бионеорганическим соединениям, так как состоит из органической части – аденозина и неорганической части – трёх связанных в цепь фосфатных групп. При рН ³ 7,0 АТФ существует в виде аниона АТФ 4- , так как все фосфатные группы при этом значении водородного показателя ионизированы.
Гидролиз АТФ записывают в виде кислотно-основного равновесия::
АТФ 4- + Н2О Û АДФ 3- + НРО4 2- + Н +
DG о = -30,5 кДж/моль,
где АДФ 3- — анион аденозидифосфата.
Как видно, гидролиз соповождается убылью энергии Гиббса
(DG о = -30,5 кДж/моль). Гидролиз может идти и дальше до образования аденозинмонофосфата (АМФ) и, наконец, до аденозина.

В химической формуле они традиционно обозначаются знаком
(тильда). В молекуле АДФ только одна высокоэнергетическая связь; в результате синтеза АТФ путём окилительного фосфорилирования добавляется ещё одна, т.е. энергия окисления субстрата трансформируется в энергию химических связей в молекуле АТФ.
Энергия, освобождающаяся при реакциях гидролиза разных веществ, обычно невелика. Если она превышает 30 кДж/моль, то гидролизуемая связь называется высокоэнергетической. Энергия гидролиза АТФ в зависимости от от локализации в клетке может меняться от 40 до 60 кДж/моль. В среднем её принято считать равной 50 кДж/моль.
В таблице 2 представлены значения стандартной энергии Гиббса гидролиза некоторых органических фосфатов.
Таблица 2: Стандартные энергии Гиббса гидролиза бионеорганических соединений
| Соединение | DG о , кДж/моль |
| Фосфоенолпируват | -61,9 |
| Ацетилфосфат | -43,1 |
| Креатинфосфат | -43,1 |
| Пирофосфат | -33,5 |
| АТФ | -30,5 |
| АТФ | -30,5 |
| Глюкозо-1-фосфат | -20,9 |
| АМФ | -14,2 |
| Глюкозо-6-фосфат | -13,8 |
| Глицеро-1-фосфат | -9,2 |
Из данных этой таблицы видно. Что гидролиз одних фосфатов приводит к высвобождению несколько большей энергии, чем гидролиз АТФ, других – меньшей.
Главный путь синтеза АТФ из АДФ – окислительное фосфорилирование. При этом АДФ фосфорилируется неорганическим фосфатом.:
Реакция энергетически сопряжена с переносом водорода с восстановленных коферментов на кислород. При этом переносе освобождается основная часть энергии окисляемых. Энергия синтеза воды из газообразных Н2 и О2 составляет 230 кДж/моль. Практически столько же получается, если используется водород. Входящий в состав органических соединений. Энергетическое сопряжение реакций переноса водорода и синтеза АТФ происходит при участии митохондриальной мембраны и Н + -АТФ-синтетазы.
Другой путь синтеза АТФ из АДФ – субстратное фосфорилирование. В этом случае механизм сопряжения не требует участия мембран.
Сущность же гидролиза заключается в переносе фосфатных групп от соединений, которые при гидролизе выделяют больше энергии, чем АТФ, к фосфорилированным соединениям, выделяющим меньше свободной энергии при гидролизе, чем АТФ.
Следовательно, АТФ функционирует в клетках как промежуточный продукт, переносящий энергию и сопрягающий реакции, сопровождающиеся выделением и потреблением энергии.
|
|

|
|
АТФ, в свою очередь, под действием другого фермента переносит концевую фосфатную группу на молекулы органических соединений с меньшей энергией, чем АТФ, тем самым запасая в них энергию. При этом вновь образуется АДФ:
где R1-фосфат – фосфорорганическое соединение с более высокой энергией, чем АТФ; R2-фосфат – фосфорорганическое соединение с более низкой энергией, чем АДФ.
Энергия гидролиза АТФ в свою очередь используется для обеспечения разнообразных эндергонических процессов. Реакция фосфорилирования АДФ и последующего использования АТФ в качестве источника энергии образует циклический процесс:
Энергия окисляемых веществ

 |  | ||||||
|
|
|
|
Рассмотренные примеры доказывают колоссальную роль гидролиза в процессах жизнедеятельности организма: На нём основываются процессы питания и выделения, поддержания гомеостаза (постоянства среды) и перераспределния энергии.
Список использованной литературы:
1. Николаев А. Я. Биологическая химия – М.: ООО «Медицинское информационное агенство», 1998.
2. Глинка Н. Л. Общая химия. Изд.19-е. «Химия», 1977.
3. Степаненко Б. Н. Курс органической химии. 3-е издание. М.: Высшая школа, 1979
4. Большая медицинская эндиклопедия. М.:«Советская энциклопедия», 1979.
5. Общая химия. Биофизическая химия. Химия биогенных элементов. М.: Высшая школа, 1993 г
Источник