Химические связи
Химическая связь — связь между атомами в молекуле или молекулярном соединении, возникающая в результате переноса электронов с одного атома на другой, либо обобществления электронов для обоих атомов.
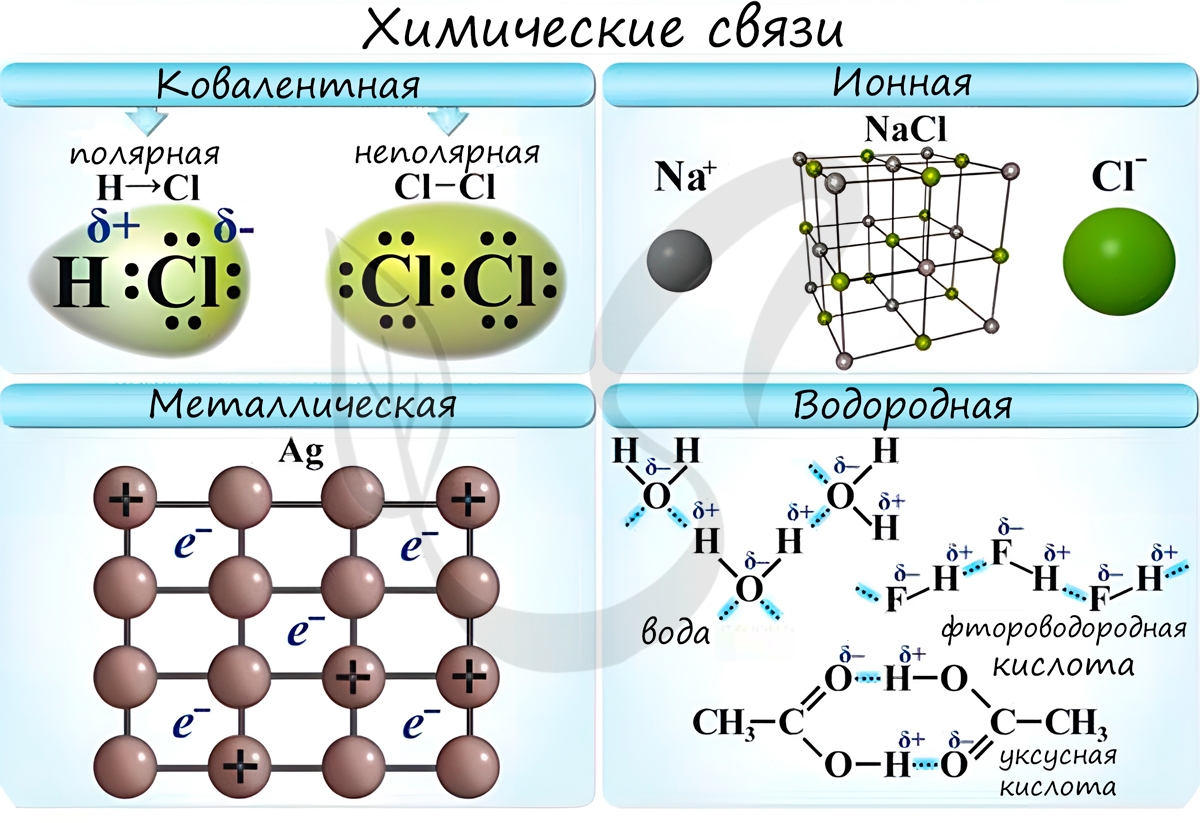
Различают несколько типов химических связей: ковалентная, ионная, металлическая, водородная.
Ковалентная связь ( лат. со — совместно + valens — имеющий силу)
Ковалентная связь возникает между двумя атомами по обменному механизму (обобществление пары электронов) или донорно-акцепторному механизму (электронов донора и свободной орбитали акцептора).
Ковалентной связью соединены атомы в молекулах простых веществ (Cl2, Br2, O2), органических веществ (C2H2), а также, в общем случае, между атомами неметалла и другого неметалла (NH3, H2O, HBr).
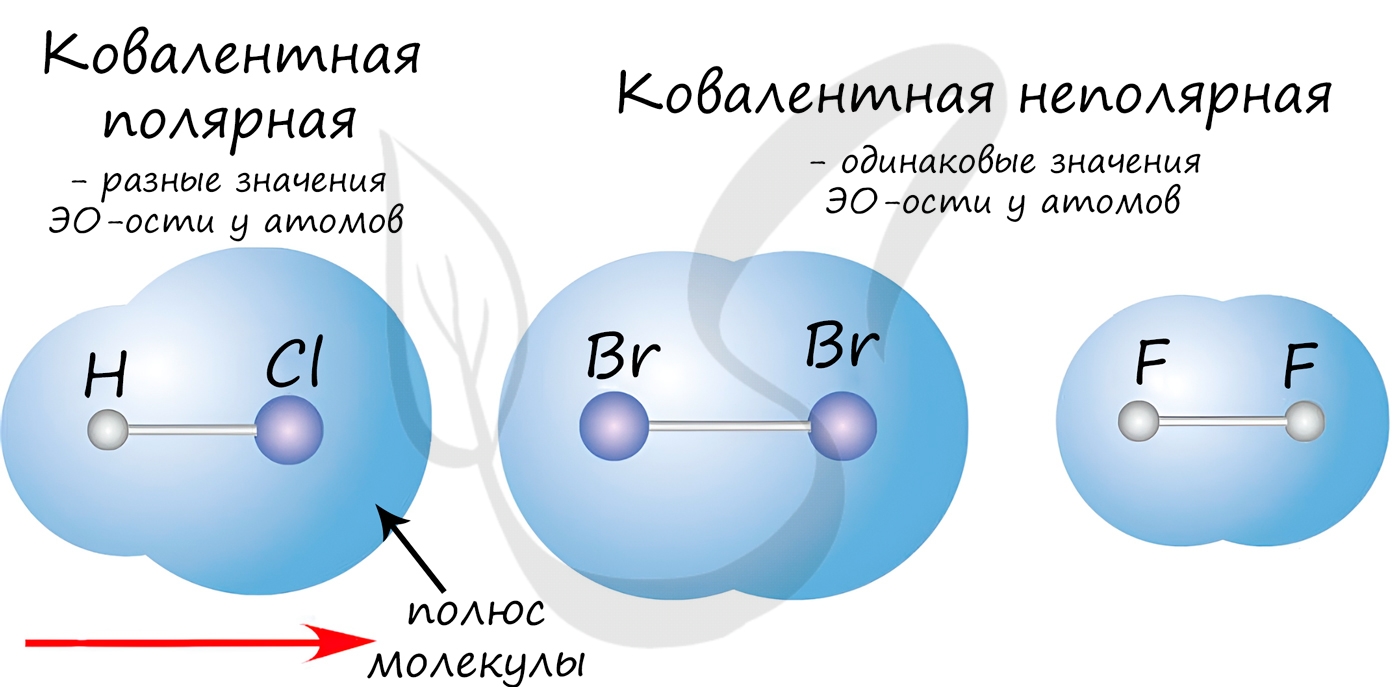
Если атомы, образующие ковалентную связь, имеют одинаковые значения электроотрицательности, то связь между ними называется ковалентной неполярной связью. В таких молекулах нет «полюса» — электронная плотность распределяется равномерно. Примеры: Cl2, O2, H2, N2, I2.
Если атомы, образующие ковалентную связь, имеют разные значения электроотрицательности, то связь между ними называется ковалентной полярной. В таких молекулах имеется «полюс» — электронная плотность смещена к более электроотрицательному элементу. Примеры: HCl, HBr, HI, NH3, H2O.
Ковалентная связь может быть образована по обменному механизму — обобществлению электронной пары. В таком случае каждый атом «одинаково» вкладывается создание связи. Например, два атома азота, образующие молекулу N2, отдают по 3 электрона с внешнего уровня для создания связи.
Существует донорно-акцепторный механизм образования ковалентной связи, при котором один атом выступает в качестве донора неподеленной электронной пары. Другой атом не тратит свои электроны, а только лишь предоставляет орбиталь (ячейку) для этой электронной пары.
Рекомендую выучить список веществ, образованных по донорно-акцепторному механизму:
- NH4 + — в ионе аммония
- NH4 + Cl, NH4 + Br — внутри иона аммония во всех его солях
- NO3 — — в нитрат ионе
- KNO3, LiNO3 — внутри нитрат иона во всех нитратах
- O3 — озон
- H3O + — ион гидроксония
- CO — угарный газ
- K[Al(OH)4], Na2[Zn(OH)4] — во всех комплексных солях есть хотя бы одна ковалентная связь, возникшая по донорно-акцепторному механизму
Ионная связь
Ионная связь — один из видов химической связи, в основе которого лежит электростатическое взаимодействие между противоположно заряженными ионами.
В наиболее частом случае ионная связь образуется между типичным металлом и типичным неметаллом. Примеры:
Большой подсказкой служит таблица растворимости, ведь все соли имеют ионные связи: CaSO4, Na3PO4. Даже ион аммония не исключение, между катионом аммония и различными анионами образуются ионные связи, например в соединениях: NH4I, NH4NO3, (NH4)2SO4.
Часто в химии встречаются несколько связей внутри одной молекулы. Рассмотрим, например, фосфат аммония, обозначив тип каждой связи внутри этой молекулы.
Металлическая связь
Металлическая связь — вид химической связи удерживающая вместе атомы металла. Этот тип связи выделен отдельно, так как его отличием является наличие высокой концентрации в металлах электронов проводимости — «электронного газа». По природе металлическая связь близка к ковалентной.
«Облако» электронов в металлах способно приходить в движение под различным воздействием. Именно оно является причиной электропроводности металлов.
Водородная связь
Водородная связь — вид химической связи, образующийся между некоторыми молекулами, содержащими водород. Одна из наиболее частых ошибок считать, что в самом газе, водороде, имеются водородные связи — это вовсе не так.
Водородные связи возникают между атомом водорода и другим более электроотрицательным атомом (O, S, N, C).
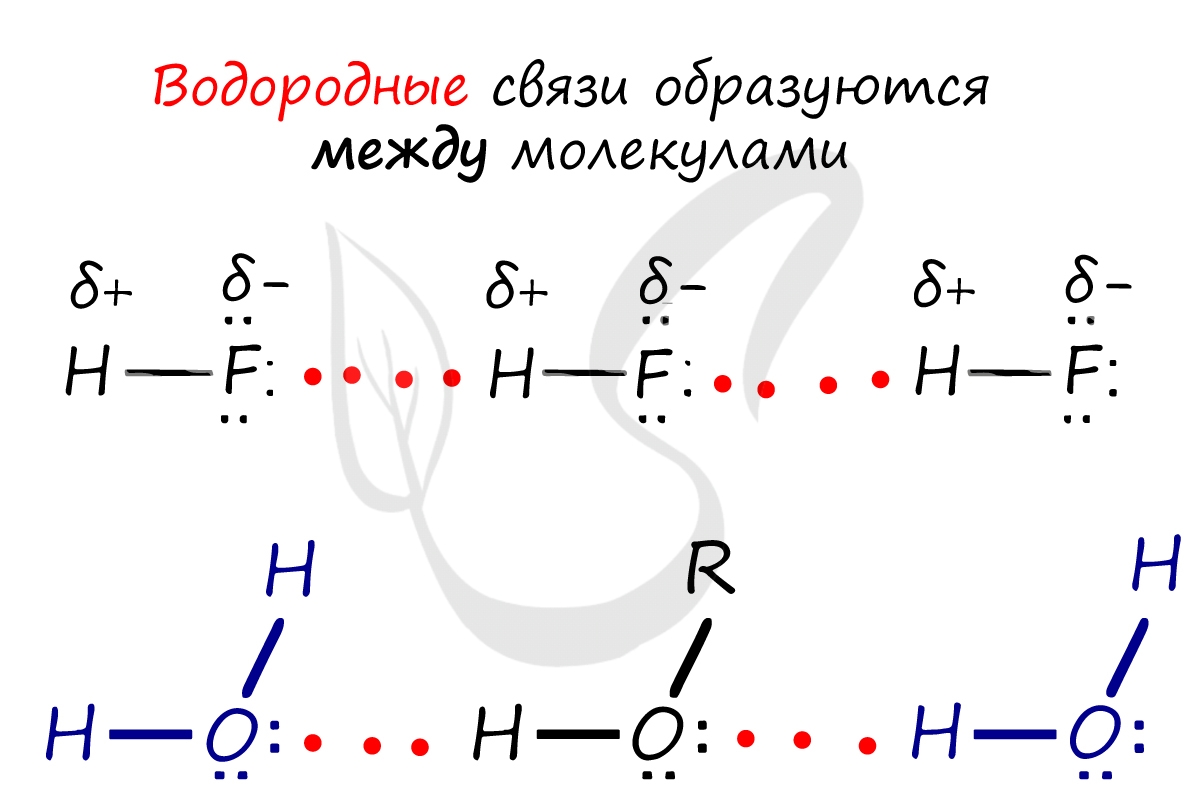
Необходимо осознать самую важную деталь: водородные связи образуются между молекулами, а не внутри. Они имеются между молекулами:
- H2O
- NH3
- HF
- Органических спиртов: С2H5OH, C3H7OH
- Органических кислот: CH3COOH, C2H5COOH
Отчасти за счет водородных связей наблюдается то самое исключение, связанное с усилением кислотных свойств в ряду галогеноводородных кислот: HF → HCl → HBr → HI. Фтор является самым ЭО-ым элементов, сильно притягивает к себе атом водорода другой молекулы, что снижает способность кислоты отщеплять водород и снижает ее силу.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Водородная связь.
Водородная связь – связь между положительно заряженным атомом водорода одной молекулы и отрицательно заряженным атомом другой молекулы.
Механизм возникновения водородной связи – частично электростатический и частично донорно-акцепторный.
Характерной чертой водородной связи является расстояние между атомом водорода и другим атомом, её образующим. Оно должно быть меньше, чем сумма радиусов этих атомов.
Водородная связь подразделяется:
1. Межмолекулярная водородная связь образуется между молекулами веществ, в состав которых входят водород и сильно электроотрицательный элемент – фтор, кислород, азот, хлор, сера. Сильно смещенная общая электронная пара от водорода к атому отрицательно заряженного элемента, при этом положительный заряд водорода сконцентрирован в малом объеме, приводит взаимодействие протона с неподеленной электронной парой другого атома или иона, обобществляя её.
Водородную связь обозначают точками, указывая, что она намного слабее ковалентной связи (примерно в 15-20 раз).
Межмолекулярная водородная связь: две молекулы воды и две молекулы уксусной кислоты с образованием циклической структуры
2. Внутримолекулярная водородная связь присутствует в многоатомных спиртах, углеводах, белках и других органических веществах.
Молекула салициловой кислоты.
Вещества с водородной связь имеют молекулярные кристаллические решетки, в узлах которой находятся молекулы.
Примеры: вода в виде льда, йод, хлор, бром, «сухой лёд» (твердый диоксид углерода), твёрдый аммиак, а также твёрдые органические вещества (метан, бензол, фенол, нафталин, белки и т.д.).
Физические свойства веществ с водородной связью.
Водородная связь обеспечивает низкомолекулярным веществам способность быть при обычных условиях в жидком агрегатном состоянии (этанол, метанол, вода) или сжижающимися газами (аммиак, фтороводород).
Более высокая температура кипения воды (100 о С) по сравнению с водородными соединениями элементов подгруппы кислорода (Н2S, Н2Sе, Н2Те), так как затрачивается дополнительная энергия на разрушение водородных связей.
Также при плавлении воды её плотность возрастает. Это объясняется тем, что в структуре льда каждый атом кислорода связан через атомы водорода с четырьмя другими атомами кислорода других молекул воды. В результате образуется рыхлая «ажурная» структура.
Источник
Вода способна образовывать ионные связи
Из предложенного перечня выберите два вещества, для которых характерна водородная связь.
Запишите в поле ответа номера выбранных соединений.
Межмолекулярная водородная связь образуется между атомом водорода, ковалентно связанным с атомом с высокой электроотрицательностью (,
и
), одной молекулы и атомом эле-мента с высокой электроотрицательностью (
,
,
) другой молекулы. Например, между атомом водорода одной молекулы фтороводорода и атомом фтора другой молекулы фтороводорода образуется водородная связь.
Среди предложенных веществ кислород в составе группы −ОН присутствует только в молекулах спиртов и фенолов, поэтому среди предложенных веществ водородная связь возможна между молекулами спиртов и фенолов. Остальные вещества относятся к углеводородам и не способны к образованию водородных связей.
Из предложенного перечня выберите два вещества, в которых между молекулами образуется водородная связь.
1)
2)
3)
4)
5)
Запишите в поле ответа номера выбранных веществ.
Водородная связь — это особый вид связи между частично положительно заряженным водородом связанным с электроотрицательным атомом (,
или
) одной молекулы (или, для внутримолекулярной связи, одной части молекулы) и частично отрицательно заряженным атомом азота, кислорода или фтора другой молекулы (или другой части молекулы).
1. В молекуле метана электроотрицательности атомов водорода и углерода близки, поэтому практически нет перераспределения заряда.
2. В молекуле фтороводорода есть частично отрицательно заряженный фтор и частично положительно заряженный водород, что позволяет образовывать водородную связь.
3. Молекула водорода содержит ковалентную неполярную связь, поэтому нет перераспределения заряда
4. В молекуле ацетальдегида электроотрицательности атомов водорода и углерода близки, поэтому практически нет перераспределения заряда, а кислород имеет сильный отрицательный заряд.
5. В молекуле перекиси водорода есть частично отрицательно заряженный кислород и частично положительно заряженный водород, что позволяет образовывать водородную связь.
Источник
Вода способна образовывать ионные связи
Из предложенного перечня выберите два типа химических связей, которые реализуются в сульфате калия.
1) ковалентная неполярная
2) ковалентная полярная
Запишите в поле ответа номера выбранных соединений.
Ковалентная неполярная связь образуется в молекулах между атомами одного элемента-неметалла. Ковалентная полярная связь образуется в молекулах между атомами разных неметаллов, ионная — между атомами металлов и неметаллов.
В сульфате калия между ионами калия и сульфат-ионами связь ионная, а между кислородом и серой в сульфат-ионе — ковалентная полярная.
Химическая связь между молекулами воды
3) ковалентная полярная
4) ковалентная неполярная
Ковалентная связь образуется между атомами, ионная — между ионами.
Между молекулами существует межмолекулярное взаимодействие, одной из форм которого является водородная связь.
Межмолекулярная водородная связь образуется между атомом водорода, ковалентно связанным с атомом с высокой электроотрицательностью (F, O и N), одной молекулы и атомом элемента с высокой электроотрицательностью (F, O, N, Cl) другой молекулы. Например, между атомом водорода одной молекулы воды и атомом кислорода другой молекулы воды образуется водородная связь (обозначена пунктиром).
Каждая молекула воды может образовать четыре водородные связи — две за счет двух атомов водорода и две за счет двух неподеленных электронных пар атома кислорода.
Из предложенного перечня выберите две химические связи, образованные между атомами с одинаковой относительной электроотрицательностью.
2) ковалентная полярная
3) ковалентная неполярная
Запишите в поле ответа номера выбранных химических связей.
Между атомами с одинаковой относительной электроотрицательностью может образоваться ковалентная неполярная или металлическая связь.
В хлориде аммония присутствуют химические связи:
2) ковалентные полярные
3) ковалентные неполярные
Запишите в таблицу номера выбранных ответов.
Это соль, поэтому присутствуют ионные химические связи, а в ионе аммония — ковалентные полярные.
В сульфате калия присутствуют химические связи:
2) ковалентные неполярные
3) ковалентные полярные
Запишите номера выбранных ответов.
Это соль, поэтому присутствуют ионные химические связи, а в сульфатном анионе — ковалентные полярные.
Химическая связь в молекулах метана и хлорида кальция соответственно
1) ковалентная полярная и металлическая
2) ионная и ковалентная полярная
3) ковалентная неполярная и ионная
4) ковалентная полярная и ионная
Ковалентная полярная связь образуется в молекулах между атомами разных неметаллов, ионная — между атомами металлов и неметаллов. Определим состав веществ по формулам: в метане — углерод и водород, поэтому связь ковалентная полярная, в хлориде кальция — кальций и хлор, значит, связь ионная.
вопрос составлен некорректно ,варианты ответов 2 и 4 полностью идентичны
нет, всё дело в слове «соответственно»
Химическая связь в метане и хлориде кальция соответственно
1) ковалентная полярная и металлическая
2) ионная и ковалентная полярная
3) ковалентная неполярная и ионная
4) ковалентная полярная и ионная
Метан имеет ковалентную полярную связь, а хлорид кальция — типичная соль — ионную.
Из предложенного перечня выберите две химические связи, образованные в молекуле водорода.
3) ковалентная полярная
5) ковалентная неполярная
Запишите в поле ответа номера выбранных химических связей.
Ковалентная неполярная связь образуется в молекулах между атомами одного элемента-неметалла. Ковалентная полярная связь образуется в молекулах между атомами разных неметаллов, ионная — между атомами металлов и неметаллов. Поэтому химическая связь в молекуле водорода одинарная ковалентная неполярная.
В твердых веществах молекулярного строения химическая связь между молекулами
4) ван-дер-ваальсова или водородная
В твердых веществах молекулярного строения взаимодействие осуществляется между нейтральными молекулами это межмолекулярное взаимодействие называется ван-дер-ваальсовой связью.
В некоторых веществах между молекулами возникают водородные связи (вода, аммиак, фтороводород. )
Почему ответ не 1, ведь в прошлом задании было сказано:» Вещества, в молекулах которых атомы соединены ковалентными связями могут иметь молекулярные и атомные кристаллические решетки.»
Здесь спрашивают про «связь между молекулами», а не между атомами в молекуле.
Какая химическая связь образуется между атомами элементов с порядковыми номерами 9 и 19?
3) ковалентная полярная
4) ковалентная неполярная
Ковалентная связь это соединение атомов посредством общих электронных пар, образуется между атомами неметаллов. Ионная связь это связь между ионами, образуется при взаимодействии атомов металла и неметалла. Элемент №9 это неметалл фтор. Элемент №19 это металл калий, поэтому связь ионная.
Химическая связь в бромиде натрия
1) ковалентная неполярная
3) ковалентная полярная
Ковалентная неполярная связь образуется в молекулах между атомами одного элемента-неметалла. Ковалентная полярная связь образуется в молекулах между атомами разных неметаллов, ионная — между атомами металлов и неметаллов. Поэтому химическая связь в бромиде натрия ионная.
Из предложенного перечня выберите два вещества, для которых характерна водородная связь.
Запишите в поле ответа номера выбранных соединений.
Межмолекулярная водородная связь образуется между атомом водорода, ковалентно связанным с атомом с высокой электроотрицательностью (,
и
), одной молекулы и атомом эле-мента с высокой электроотрицательностью (
,
,
) другой молекулы. Например, между атомом водорода одной молекулы фтороводорода и атомом фтора другой молекулы фтороводорода образуется водородная связь.
Среди предложенных веществ кислород в составе группы −ОН присутствует только в молекулах спиртов и фенолов, поэтому среди предложенных веществ водородная связь возможна между молекулами спиртов и фенолов. Остальные вещества относятся к углеводородам и не способны к образованию водородных связей.
Источник