- Вода как растворитель
- Процесс растворения
- Значение воды для жизни живых существ
- Свойства воды, важные для биологии человека
- 1- Вода как растворитель
- 2- В потоке движения молекул воды через биологические мембраны
- 3- Вода во многих химических реакциях
- 4- Роль воды как смазки
- 5- Тепловые свойства воды способствуют жизни
- Универсальный растворитель – определение и характеристики
- Универсальное определение растворителя
- Характеристики универсального растворителя
- полярность
- Высокая удельная теплоемкость
- Уникальные свойства плотности и температуры
- викторина
Вода как растворитель

Вследствие своих аномальных свойств вода уникальный растворитель, прекрасно приспособленный для жизнедеятельности.

Другой многочисленный класс веществ, хорошо растворимых в воде, включает такие полярные органические соединения, как сахара, альдегиды, кетоны, спирты. Их растворимость в воде объясняется склонностью молекул воды к образованию полярных связей с полярными функциональными группами этих веществ, например с гидроксильными группами спиртов и сахаров или с атомом кислорода карбонильной группы альдегидов и кетонов. Ниже приведены примеры водородных связей, важных для растворимости веществ в биологических системах. Вследствие высокой полярности вода вызывает гидролиз веществ.
Так как вода составляет основную часть внутренней среды организма, то она обеспечивает процессы всасывания, передвижения питательных веществ и продуктов обмена в организме.
Необходимо отметить, что вода является конечным продуктом биологического окисления веществ, в частности глюкозы. Образование воды в результате этих процессов сопровождается выделением большого количества энергии приблизительно 29 кДж/моль.
Важны и другие аномальные свойства воды: высокое поверхностное натяжение, низкая вязкость, высокие температуры плавления и кипения и более высокая плотность в жидком состоянии, чем в твердом.
Для воды характерно наличие ассоциатов групп молекул, соединенных водородными связями.
В зависимости от сродства к воде функциональные группы растворяемых частиц подразделяются на гидрофильные (притягивающие воду), легко сольватируемые водой, гидрофобные (отталкивающие воду) и дифильные.
К гидрофильным группам относятся полярные функциональные группы: гидроксильная —ОН, амино —NH2 , тиольная —SH, карбоксильная —СООН.
К гидрофобным — неполярные группы, например углеводородные радикалы: СНз—(СН2)п —, С6Н5 —.
К дифильным относят вещества (аминокислоты, белки), молекулы которых содержат как гидрофильные группы (—ОН, —NH2 , —SH, —СООН), так и гидрофобные группы: (СН3, (СН2)п ,—С6Н5—).
При растворении дифильных веществ происходит изменение структуры воды как результат взаимодействия с гидрофобными группами. Степень упорядочения молекул воды, близко расположенных к гидрофобным группам, увеличивается, и контакт молекул воды с гидрофобными группами сводится к минимуму. Гидрофобные группы, ассоциируясь, выталкивают молекулы воды из области своего расположения.
Процесс растворения
Природа процесса растворения сложна. Естественно, возникает вопрос, почему некоторые вещества легко растворяются в одних растворителях и плохо растворимы или практически нерастворимы в других.

Великий русский химик Д. И. Менделеев (1834—1907) считал, что важную роль при растворении играют химические процессы. Он доказал существование гидратов серной кислоты H2SО4*H2O, H2SО4*2H2O, H2SО4*4H2О и некоторых других веществ, например, С2Н5ОН*3Н2О. В этих случаях растворение сопровождается образованием химических связей частиц растворяемого вещества и растворителя. Этот процесс называется сольватацией, в частном случае, когда растворителем является вода, гидратацией.
Как установлено, в зависимости от природы растворенного вещества сольваты (гидраты) могут образовываться в результате физических взаимодействий: иондипольного взаимодействия (например, при растворении веществ с ионной структурой (NaCI и др.); дипольдипольного взаимодействия при растворении веществ с молекулярной структурой (органические вещества)).
Химические взаимодействия осуществляются за счет донорноакцепторных связей. Здесь ионы растворенного вещества являются акцепторами электронов, а растворители (Н2О, NН3) донорами электронов (например, образование аквакомплексов), а также в результате образования водородных связей (например, растворение спирта в воде).

Например, при растворении гидроксида калия в воде выделяется теплота:
А при растворении хлорида натрия теплота поглощается:
Теплота, выделяемая или поглощаемая при растворении 1 моля вещества, называется теплотой растворения Qраств
В соответствии с первым началом термодинамики
где ΔНраств изменение энтальпии при растворении данного количества вещества.
Растворение в воде безводного сульфата меди белого цвета приводит к появлению интенсивной голубой окраски. Образование сольватов, изменение окраски, тепловые эффекты, как и ряд других факторов, свидетельствуют об изменении химической природы компонентов раствора при его образовании.
Таким образом, в соответствии с современными представлениями, растворение физико-химический процесс, в котором играют роль как физические, так и химические виды взаимодействия.
Источник
Значение воды для жизни живых существ
Вода важна для жизни и его процесс, потому что он является основным компонентом большинства организмов на Земле. Многие организмы состоят из 95% воды; почти все остальные состоят из половины воды. Кроме того, две трети планеты покрыты водой.
Вода обладает множеством уникальных свойств. Это единственное вещество, которое находится в жидкой форме при температуре, обычно встречающейся на планете Земля. Кроме того, это отличный растворитель, а это значит, что многие вещества могут растворяться в нем. Это позволяет воде транспортировать питательные вещества к живым клеткам, а также помогает избавиться от их отходов..
Вода также регулирует деятельность в жидкостях, тканях, клетках, лимфе, крови и железах человека.
Для живых существ необходимо пить воду, чтобы остаться в живых. Взрослый человек содержит около 42 литров воды. С потерей всего 2,7 литра человек может страдать от симптомов обезвоживания. Эти симптомы включают головокружение, слабость, головные боли, усталость и нервозность. В крайних случаях обезвоживание может вызвать смерть.
Вода циркулирует естественным образом на поверхности Земли, поскольку она циркулирует по всему человеческому телу; транспортирует, растворяет, пополняет питательные и органические вещества, удаляя ненужные материалы.
В заключение, вода играет очень важную роль для жизни, а также имеет много функций в химии, биохимии и биологии благодаря своим разнообразным свойствам. Его физические свойства относятся к его тепловым свойствам и химическим свойствам, поскольку он взаимодействует с другими веществами..
Может быть, вы заинтересованы в состоянии воды: твердые, жидкие и газовые.
Свойства воды, важные для биологии человека
1- Вода как растворитель
Вода является отличным растворителем. Это означает, что многие различные материалы могут быть растворены в нем для образования растворов. Вода — это растворитель, который несет много незаменимых молекул и других частиц по всему телу. Это включает в себя питательные вещества и продукты жизнедеятельности, вырабатываемые в процессе обмена веществ организма.
2- В потоке движения молекул воды через биологические мембраны
Некоторые частицы и молекулы, такие как ионы, должны иметь возможность перемещаться вокруг биологических организмов, таких как ткани и мембраны. Один из способов, которым это происходит, заключается в решениях. Примеры этого включают транспортировку кислорода в крови вокруг сосудистой системы..
Движения растворов в четко определенных каналах, таких как сосуды и лимфатическая система, легко объяснить по сравнению с движениями жидкостей по трубопроводам..
3- Вода во многих химических реакциях
Химические реакции происходят только тогда, когда реагенты вступают в контакт с самими собой, иногда через промежуточные стадии с участием катализаторов..
Растворы обычно являются хорошими переносчиками для химических реакций, поскольку растворитель, в данном случае вода, заключает в капсулы растворенные вещества, которые могут быть потенциальными реагентами, если есть какая-либо возможность их реакции друг с другом. Когда два или более реагентов находятся в одном и том же растворе, они могут столкнуться и вызвать реакцию.
Возможность этого зависит от многих факторов, включая концентрацию растворенных веществ, температуру раствора и наличие катализатора для реакции..
Молекулы воды также участвуют в реакциях разложения, когда определенные молекулы делятся на более мелкие части. Примеры этого включают обработку углеводов и белков во время процесса пищеварения.
Вода также происходит в некоторых химических реакциях, которые происходят в организме. В этих реакциях небольшие органические соединения собираются вместе, образуя более крупные и более сложные молекулы, необходимые организму для выполнения определенных функций, таких как образование нуклеиновых кислот и гормонов..
4- Роль воды как смазки
Смазка уменьшает трение между движущимися поверхностями. Вода, включая растворы, в которых вода является растворителем, играет важную роль в смазочных функциях. Это важно во многих частях тела, таких как:
- В грудной и брюшной полостях. В этой области внутренние органы, такие как сердце, легкие и пищеварительная система, расположены рядом и скользят друг с другом при движении тела..
- В суставах. В этой области такие структуры, как кости, связки и сухожилия, должны свободно перемещаться. Эти части относительно близко друг к другу и нуждаются в чем-то, что предотвращает трение, возникающее между различными конструкциями и поверхностями..
5- Тепловые свойства воды способствуют жизни
Вода имеет определенную точку нагрева. Удельная теплоемкость вещества — это количество тепла на единицу массы, необходимое для повышения температуры вещества на один градус Цельсия..
По сравнению с другими растворителями, для повышения температуры воды требуется больше энергии. Это происходит потому, что водород удерживает молекулы воды вместе. Тепловые свойства воды, которые влияют на биологию животных и человека, включают:
- По сравнению с другими материалами вода может поглощать или избавляться от относительно большого количества тепловой энергии при минимальной регулировке собственной температуры..
Большое количество человеческого тела состоит из воды. Следовательно, эта способность помогает организму справляться с колебаниями температуры окружающей среды. Кроме того, это помогает поддерживать организм в комфортном и безопасном для человека диапазоне температур..
- Кроме того, по сравнению с другими материалами воде также требуется относительно большое количество тепловой энергии для испарения..
Это означает, что испарение пота на коже является очень эффективным механизмом для охлаждения тела; удаляет большое количество тепла тела при испарении пота.
Источник
Универсальный растворитель – определение и характеристики
Универсальное определение растворителя
Вода это вещество, которое мы называем универсальным растворитель, Растворитель – это просто жидкость, в которой могут растворяться другие вещества, и причина, по которой вода получила ярлык универсального растворителя, заключается в том, что никакой другой растворитель не может растворить столько веществ, сколько может. Это в основном то, что делает его таким важным для жизни на земле. Кроме того, удивительно, что каждый водоем, найденный на земле, включая лед, поддерживает ту или иную форму жизни, которая адаптировалась к температуре и давлению, обнаруженному в этой форме воды.
Тот простой факт, что ученым всегда интересно находить воду, связанную с жизнью, на других планетах, многое говорит об этом, казалось бы, простом веществе. Вода является наиболее распространенным веществом в организмах и клетках. Конечно, есть много очевидных применений для воды, таких как питье, мытье и тушение пожаров, и это благодаря характеристикам, которыми он обладает, которые делают его универсальным растворителем. Вода очень важна для жизни, потому что для многих важных реакций в организме организмов необходима водная среда. Например, вода необходима для переваривания белков в аминокислоты, И в фотосинтез и пищеварение.
Характеристики универсального растворителя
полярность
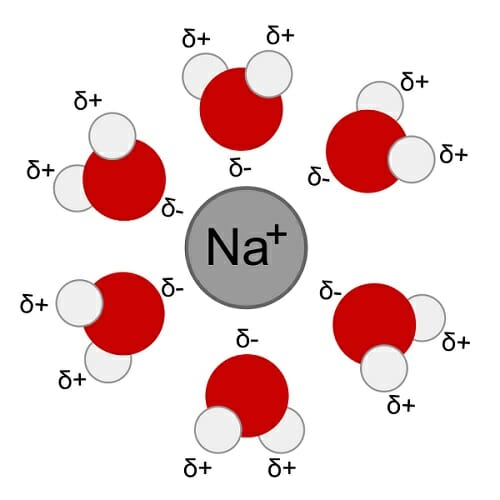
Это большая часть того, почему вода является универсальным растворителем. Полярность – это неравномерность распределения электронов в молекула, что приводит к одной молекуле, имеющей две противоположные стороны; один отрицательный и один положительный. Теперь вода имеет молекулярную формулу H2O, поэтому каждая молекула воды имеет два атома водорода и один атом кислорода, как вы можете видеть на диаграмме ниже. Атомы водорода не находятся на противоположных сторонах друг друга, и они несут частичный положительный заряд. Это означает, что они создают положительно заряженную часть молекулы, в то время как кислородный конец создает отрицательно заряженную часть. Эта полярность означает, что вода может присоединяться и, следовательно, растворять полярные и ионные (заряженные) вещества.
Высокая удельная теплоемкость
Количество энергии, необходимое для повышения температуры одного грамма воды на 1 градус Цельсия, является ее удельной теплотой, и при одной калории на грамм она намного выше, чем удельная теплоемкость большинства жидкостей. Это хорошая новость для нас, так как мы на 60% состоим из воды, и мы не смогли бы выжить, если бы наши тела сильно и быстро остыли и нагрелись. Это также имеет решающее значение для выживания всех других организмов, в том числе водных организмов. Это означает, что океаны и реки не замерзают постоянно или не испаряются при изменении температуры. Если вода не может стабилизировать свою температуру, энергия, которая выделяется во время обмена веществ в живых организмах, может привести к перегреву и смерти.
Уникальные свойства плотности и температуры
Когда мы помещаем кубик льда в воду, он плавает, и, к счастью, то же самое относится и к айсбергу. Если бы лед был более плотным, чем вода, он бы постоянно замерзал наверху, а затем опускался, пока все водоемы не превратятся в лед, уничтожая всю жизнь. Вода также существует в виде газа, жидкости и твердого вещества в очень небольшом диапазоне температур, что означает, что мы можем найти ее во всех трех формах на Земле в зависимости от того, где мы находимся, и часто в одном и том же месте. Это не часто встречающаяся собственность.
- растворенное вещество – Это вещество, которое растворяется в другом растворителе.
- Ковалентная связь – Распределение электронов между атомами с образованием молекулы.
- Круговорот воды – Процесс циркуляции воды между различными элементами земли – атмосферой, землей и океанами.
- метаболизм – Все химические реакции, происходящие внутри живых организмов.
викторина
1. Вода считается полярной, потому что:A. У этого есть одна отрицательная сторона и другая, которая является положительной.B. Это универсальный растворитель.C. У него два атома водорода.D. Это самый плотный в твердой форме.
Ответ на вопрос № 1
верно. У воды есть сторона, которая немного положительна, и сторона, которая слегка отрицательна.
2. Что из следующего является силой, которая удерживает молекулы воды вместе?A. Ковалентные связи B. Ионные связиC. Полярные связиD. Водородные связи
Ответ на вопрос № 2
D верно. Водородные связи образуются между атомами кислорода и атомами водорода различных молекул воды.
3. Какое свойство относится к слипшимся молекулам воды?A. прилипание B. полярностьC. когезияD. Быть универсальным растворителем
Ответ на вопрос № 3
С верно. Силы сцепления, вызванные водородными связями, делают воду эластичной.
Источник