- 5 аномальных фактов о воде
- Может ли вода оставаться жидкой при температуре ниже нуля?
- Давление
- Добавки
- Другие методы. Переохлаждённая вода
- Исследование свойств воды при кристаллизации
- Вступление
- Введение
- 1. Подготовка к исследованию
- 1.1 Анализ основных свойств воды
- 1.2 Значение кристаллизации воды для флоры и фауны
- 1.3 Выбор и обоснование опытов для проведения исследования
- 2. Проведение исследования
- 2.1 Подготовка материальной части
- 2.2 Проведение опытов с описанием основных результатов
- 1. Замерзание соленой воды.
- 2. Расширение воды при замерзании.
- 3. Замерзание жидкости при внешнем воздействии снега.
- 4. Замерзание мыльных пузырей.
- 5. Срастание сосульки.
- 6. Скрип сухого снега.
- 7. Примерзание к поверхности.
- 2.3 Предложения по проведению опытов
- Заключение
5 аномальных фактов о воде
Несмотря на простую химическую формулу, вода — вещество с очень необычными свойствами. Она таит в себе множество загадок, которые порой не под силу разгадать даже ученым.
Перед вами пять наиболее интересных фактов о воде.
1. Горячая вода замерзает быстрее холодной
Возьмем две емкости с водой: в одну нальем горячую, а в другую — холодную воду, и поместим их в морозильную камеру. Горячая вода замерзнет быстрее холодной, хотя по логике вещей, первой должна была превратиться в лед холодная вода: ведь горячей воде надо сначала остыть до температуры холодной, а потом уже превращаться в лед, в то время как холодной воде остывать не надо.
Почему же так происходит?
В 1963 году один танзанский студент по имени Эрасто Б. Мпемба (Erasto B. Mpemba) замораживая приготовленную смесь для мороженого, заметил, что горячая смесь застывает в морозильной камере быстрее, чем холодная. Когда юноша поделился своим открытием с учителем физики, тот лишь посмеялся над ним.
К счастью, ученик оказался настойчивым и убедил учителя провести эксперимент, который и подтвердил его открытие: в определенных условиях горячая вода действительно замерзает быстрее холодной.
Теперь этот феномен горячей воды, замерзающей быстрее холодной, носит название «эффект Мпемба». Правда, за долго до него это уникальное свойство воды было отмечено Аристотелем, Фрэнсисом Бэконом и Рене Декартом.
Ученые так до конца и не понимают природу этого явления, объясняя его либо разницей в переохлаждении, испарении, образовании льда, конвекции, либо воздействием разжиженных газов на горячую и холодную воду.
2. Сверхохлаждение и «мгновенное» замерзание
Все знают, что вода всегда превращается в лед при охлаждении до 0 °C … за исключением некоторых случаев! Таким случаем, например, является сверхохлаждение, которое представляет собой свойство очень чистой воды оставаться жидкой, даже будучи охлажденной до температуры ниже точки замерзания.
Это явление становится возможным благодаря тому, что окружающая среда не содержит центров или ядер кристаллизации, которые могли бы спровоцировать образование кристаллов льда. И поэтому вода остается в жидкой форме, даже будучи охлажденной до температуры ниже нуля градусов по Цельсию.
Процесс кристаллизации может быть спровоцирован, например, пузырьками газа, примесями (загрязнениями), неровной поверхностью емкости. Без них вода будет оставаться в жидком состоянии. Когда процесс кристаллизации запускается, можно наблюдать, как сверхохлажденная вода моментально превращается в лед.
Заметьте, что «сверхнагретая» вода также остается жидкой, даже будучи нагретой до температуры выше точки закипания.
3. «Стеклянная» вода
Не задумываясь, назовите, сколько различных состояний есть у воды? Если вы ответили три: твердое, жидкое, газообразное, то вы ошиблись. Ученые выделяют как минимум 5 различных состояний воды в жидком виде и 14 состояний в замерзшем виде.
Помните разговор про сверхохлажденную воду? Так вот, что бы вы ни делали, при температуре -38 °C даже самая чистая сверхохлажденная вода внезапно превратится в лед.
Что же произойдет при дальнейшем понижении температуры?
При -120 °C с водой начинает происходить что-то странное: она становится сверхвязкой или тягучей, как патока, а при температуре ниже -135 °C она превращается в «стеклянную» или «стекловидную» воду – твердое вещество, в котором отсутствует кристаллическая структура.
4. Квантовые свойства воды
На молекулярном уровне вода удивляет ещё больше. В 1995 году проводимый учеными эксперимент по рассеянию нейтронов дал неожиданный результат: физики обнаружили, что нейтроны, направленные на молекулы воды, «видят» на 25% меньше протонов водорода, чем ожидалось.
Оказалось, что на скорости одной аттосекунды (10 -18 секунд) имеет место необычный квантовый эффект, и химическая формула воды вместо H2O, становится H1.5O!
5. Есть ли у воды память?
Альтернативная официальной медицине гомеопатия утверждает, что разбавленный раствор лекарственного препарата может оказывать лечебный эффект на организм, даже если коэффициент разбавления настолько велик, что в растворе уже не осталось ничего, кроме молекул воды.
Сторонники гомеопатии объясняют этот парадокс концепцией под названием «память воды», согласно которой вода на молекулярном уровне обладает «памятью» о веществе, некогда в ней растворенном и сохраняет свойства раствора первоначальной концентрации после того, как в нём не остается ни одной молекулы ингредиента.
Международная группа ученых во главе с профессором Мэдлин Эннис (Madeleine Ennis) из Королевского университета в Белфасте (Queen’s University of Belfast), критиковавшая принципы гомеопатии, в 2002 году провела эксперимент, чтобы раз и навсегда опровергнуть эту концепцию.
Результат оказался обратным. После чего, ученые заявили, что им удалось доказать реальность эффекта «памяти воды». Однако опыты, проведенные под наблюдением независимых экспертов, результатов не принесли. Споры о существовании феномена «памяти воды» продолжаются.
Вода обладает множеством других необычных свойств, о которых мы не рассказали в этой статье. Например, плотность воды меняется в зависимости от температуры (плотность льда меньше плотности воды); вода обладает довольно большой величиной поверхностного натяжения; в жидком состоянии вода представляет собой сложную и динамически меняющуюся сеть из водных кластеров, и именно поведение кластеров влияет на структуру воды и т.д.
Источник
Может ли вода оставаться жидкой при температуре ниже нуля?
Да, может. Температура замерзания воды падает ниже нуля градусов по Цельсию, если вы оказываете на неё давление. И не только.
Это может произойти несколькими способами. Рассмотрим их далее.
Давление
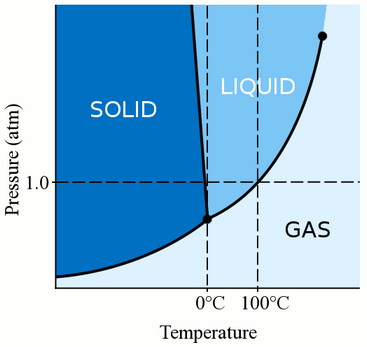
Прежде всего, фаза материала (будь то газ, жидкость или твёрдое вещество) сильно зависит как от его температуры, так и от давления.
Для большинства жидкостей давление поднимает температуру, при которой жидкость замерзает. Твёрдое тело образуется, когда свободные молекулы жидкости становятся достаточно медленными и достаточно близко располагаются друг к другу, чтобы сформировать стабильные связи, которые закрепляют их на месте. Когда мы оказываем давление на жидкость, мы заставляем молекулы сближаться. Поэтому они могут образовывать стабильные облигации и стать твёрдыми при более высокой температуре, чем температура замерзания при стандартном давлении.
Однако вода несколько уникальна.
Молекулы воды распространяются, когда они связываются в твёрдую кристаллическую структуру. Это действие делает лёд менее плотным, чем жидкостная вода, поэтому лёд плавает, а не тонет. Это действие молекул воды при замерзании также означает, что давление воды понижает температуру замерзания. Если вы примените достаточное давление (что затрудняет распространение молекул воды в твёрдую структуру), вы можете получить жидкую воду на несколько градусов ниже нуля градусов по Цельсию.
Добавки
Даже без давления вы можете получить жидкую воду при минусовой температуре, используя добавки. Такие добавки, как соль, могут помешать сформировать твёрдое тело и понизить температуру замерзания воды.
Соль состоит из сильных ионов натрия и хлора. Растворённые в воде, молекулы воды присоединяются к ионам соли, и поэтому не замерзают как охотно. По мере того, как вы добавляете больше соли в воду, точка замерзания продолжает падать, пока вода не достигнет насыщения и не сможет удерживать соль.
Если добавить достаточное количество соли, температура замерзания воды может упасть до -21 градуса Цельсия.
Этот факт означает, что вода при температуре -21 градус Цельсии может всё ещё быть жидкой (с достаточным количеством соли).
Это мощное свойство соли можно также использовать для того, чтобы дать льду превратиться обратно в воду. Посыпание солью ледяных тротуаров снижает температуру замерзания льда ниже температуры окружающей среды, и лёд тает.
Но посыпать солью обледеневшие дорожки не поможет, если температура окружающей среды ниже -21 градуса по Цельсию.
Воздействие соли на точку замерзания воды также оказывает глубокое воздействие на океаны Земли.
Другие методы. Переохлаждённая вода
Даже если вы не применяете давление и ничего не добавляете в воду, вы всё равно можете иметь жидкую воду при температуре ниже нуля градусов по Цельсию.
Для того, чтобы вода замёрзла до льда, ей нужно замёрзнуть, чтобы начать процесс. Эти отправные точки называются «центрами нуклеации». В большинстве случаев немного пыли, примесей или даже небольшие колебания в воде обеспечивают центры зарождения для замерзания воды. Но если ваша вода очень чистая и неподвижная, молекулам воды не на что кристаллизоваться. В результате вы можете охладить очень чистую воду ниже нуля градусов по Цельсию без замерзания.
Вода в таком состоянии называется «переохлаждённой».
Чистую воду можно переохладить до около -40 градус Цельсия.
Переохлаждённая вода удерживается от замерзания только отсутствием центров зарождения. Поэтому, как только появятся центры нуклеации (что может произойти от простой вибрации), супер-охлаждённая вода быстро замерзает.
Ледяной дождь — это естественный пример переохлаждённой жидкой воды. Как только дождь попадает на объект на поверхности Земли, объект обеспечивает центры нуклеации, и дождь замерзает до льда.
Какой обьект обеспечивает какие центры нуклеации? Что спрятано за этими терминами? — незнание!
Источник
Исследование свойств воды при кристаллизации
Вступление
Вода является не только одним из самых необходимых, но и самых удивительных явлений на нашей планете. Исключительно важна роль воды в возникновении и поддержании жизни на Земле, в химическом строении живых организмов, в формировании климата и погоды. Вода является важнейшим веществом для всех живых существ на Земле.
Введение
Большая часть поверхности Земли покрыта водой (океаны, моря, озёра, реки, льды). На Земле примерно 96,5 % воды приходится на океаны, 1,7 % мировых запасов составляют грунтовые воды, ещё 1,7 % – ледники и ледяные шапки Антарктиды и Гренландии, небольшая часть находится в реках, озёрах и болотах, и 0,001 % в облаках, которые образуются из взвешенных в воздухе частиц льда и жидкой воды.
Вода при нормальных условиях находится в жидком состоянии, однако при температуре в 0 °C она переходит в твердое состояние – лед и кипит (превращается в водяной пар) при температуре 100 °C.
Значения 0 °C и 100 °C были выбраны как соответствующие температурам таяния льда и кипения воды при создании температурной шкалы «по Цельсию».
Лёд встречается в природе в виде собственно льда (материкового, плавающего, подземного), а также в виде снега, инея, изморози. Под действием собственного веса лёд приобретает пластические свойства и текучесть.
Природный лёд обычно значительно чище, чем вода, так как при кристаллизации воды в первую очередь в решётку встают молекулы воды.
Общие запасы льда на Земле около 30 млн. км³. Основные запасы льда сосредоточены в полярных шапках (главным образом, в Антарктиде, где толщина слоя льда достигает 4 км).
В мировом океане вода солёная и это препятствует образованию льда, поэтому лёд образуется только в полярных и субполярных широтах, где зима долгая и очень холодная. Замерзают некоторые неглубокие моря, расположенные в умеренном поясе.
Кроме того, имеются данные о наличии льда на планетах Солнечной системы (например, на Марсе), их спутниках, на карликовых планетах и в ядрах комет.
Исследование свойств воды необходимо для человечества.
При этом процесс кристаллизации воды можно изучать в домашних условиях, а также на уроках в средней школе.
Актуальность работы использование на уроках физики, для знакомства учащихся со свойствами воды при кристаллизации.
Объектом исследования является кристаллизация воды.
Предмет исследования – изучения свойств воды при кристаллизации.
Цель работы провести опыты по кристаллизации воды и подготовить предложения по их проведению.
Главной задачей является изучение свойств воды при кристаллизации.
Для решения главной задачи необходимо:
- Повести анализ основных свойств воды.
- Изучить значение кристаллизации воды для флоры и фауны Земли.
- Определить основные опыты для проведения исследования.
- Провести опыты и описать основные результаты.
- Подготовить предложения по проведению опытов на уроках в средней школе.
Теоретическая значимость работы заключается в систематизации основных свойств воды и значения кристаллизации воды для флоры и фауны Земли.
Практическая значимость работы – изучение процесса кристаллизации воды во время проведение опытов, а также подготовка предложений по проведению опытов на уроках в средней школе.
1. Подготовка к исследованию
1.1 Анализ основных свойств воды
Вода является одним из самых удивительных веществ на планете Земля. Встретить воду можно практически везде в естественных условиях как на поверхности планеты, так и в ее недрах в трех возможных физических состояниях для веществ: жидкое, твердое, газообразное (то есть вода, лед, водяной пар).
Конечно, существуют вещества, которые можно получить в виде жидкости, твердого тела или газа. Однако, не существует подобного химического вещества, которое именно в естественных условиях встречается в указанных выше трех физических состояниях.
- Вода является веществом, которое не имеет ни цвета, ни запаха, ни вкуса.
- Вода является единственным на планете Земля известным науке веществом, встречающимся в природных условиях в трех физических состояниях: твердое тело, жидкость, газ.
- Вода является универсальным растворителем, имея возможность растворять большее количество солей, а также других веществ, чем какие-либо другие вещества.
- Вода с большим трудом поддается окислению. Вода — достаточно химически устойчива, то есть разложить ее на составные части или сжечь достаточно проблематично.
- Окислению водой поддаются практически все естественные металлы, так же под ее воздействием разрушаются особо твердые горные породы.
- При замерзании вода обладает уникальными свойствами расширения. Благодаря таким свойствам лед на воде, которая находится в виде жидкости, плавает.
- Вода, как физическое вещество, характеризуется большим сродством сама с собой. Такое сродство у воды является самым большим среди всех жидкостей. Вследствие этого вода на поверхности размещается в виде капель сферической формы, поскольку сфера обладает наименьшей при заданном объеме поверхностью.
- Замерзание воды происходит не при температурных условиях ее наибольшей плотности (при 4 градусах Цельсия), а при нуле градусов Цельсия. Это свойства пресной воды. Однако, замерзание морской воды происходит при более низких температурах: минус 1,9 градусов Цельсия, при солености 35%.
- Вода обладает очень высокой теплоемкостью, относительно мало нагреваясь при этом. Также вода обладает достаточно высокой скрытой теплотой плавления (порядка 80 кал/г), а также испарения ( порядка 540 кал/г). Вода способна поглощать значительные объемы дополнительного тепла. Температура же в процессе замерзания или при кипении остается неизменной.
- Дистиллированная вода практически не проводит электрический ток, однако наличие в воде даже небольшого количества солей значительно увеличивает ее токопроводящие свойства.
- При смешивании соли со снегом наблюдается два процесса: разрушение кристаллической структуры соли, которое происходит с поглощением тепла, и гидрация ионов. Последний процесс происходит с выделением тепла в окружающую среду. Для поваренной соли и хлористого кальция первый процесс превалирует над вторым. Поэтому при смешивании снега с этими солями происходит активный отбор тепла из окружающей среды. Ещё одна особенность соляных растворов состоит в том, что их точка замерзания ниже 0 градусов. Чтобы снег на тротуарах таял при температуре ниже 0 градусов, его посыпают этими солями.
- Снег обладает удивительным свойством – памятью. Он сохраняет следы. По следам можно, например, изучать физику. Чем крупнее животное, тем глубже от него след, следовательно, тем большее давление оно оказывает на снег. Следы собаки более глубокие, чем следы её щенков. Мыши, ласки оставляет неглубокие чёрточки. Природа снабдила копытных животных способностью раздвигать копыта и увеличивать площадь опоры. Это помогает им зимой при передвижение по заснеженному лесу и полям не так глубоко погружаться в снег.
1.2 Значение кристаллизации воды для флоры и фауны
Мы любим снег не только за то, что он дарит нам великолепные зимние пейзажи. У нашей любви к снегу немало рациональных причин. «Снег на полях — хлеб в закромах», «Зима без снега – лето без хлеба», – справедливо утверждают старинные русские пословицы. Снежный покров — это огромный запас влаги, столь необходимый полям, в то же время это своеобразное гигантское одеяло, защищающее поверхность земли от холодных ветров. Академик Б. И. Вернадский подчеркивал, что снежный покров — «не просто теплая покрышка озимых, это живительная покрышка», весной он дает талые воды, насыщенные кислородом. Известно, что количество азотистых соединений летом в почве пропорционально высоте сошедшего снежного покрова. Недаром снежная мелиорация рассматривается сегодня как одно из важнейших условий получения высоких и устойчивых урожаев.
Запасы снега существенно влияют на уровень воды в реках, определяют изменения климата на больших территориях.
Кроме того, снег является хорошим строительным материалом для различных построек на севере — от иглу (жилищ эскимосов) до больших складских помещений. Существует самая большая в мире гостиница, полностью сделанная изо льда и снега, находится она в шведской Лапландии в 200 километрах от Северного полярного круга.
Он служит основой зимних дорог и даже аэродромов.
Благодаря снегу мы каждый год любуемся сказочными зимними пейзажами, играем в снежки, строим снежные городки, крепости, катаемся на лыжах, санках, в снежном уборе приходит к нам прекрасный новогодний праздник.
Значение льда трудно недооценить. Лёд оказывает большое влияние на условия обитания и жизнедеятельности растений и животных, на разные виды хозяйственной деятельности человека. Покрывая воду сверху, лед играет в природе роль своего рода плавучего экрана, защищающего реки и водоемы от дальнейшего замерзания и сохраняющего жизнь подводному миру. Если бы плотность воды увеличивалась при замерзании, лед оказался бы тяжелее воды и начал тонуть, что привело бы к гибели всех живых существ в реках, озерах и океанах, которые замерзли бы целиком, превратившись в глыбы льда, а Земля стала ледяной пустыней, что неизбежно привело бы к гибели всего живого.
Лёд может вызывать ряд стихийных бедствий с вредными и разрушительными последствиями – обледенение летательных аппаратов, судов, сооружений, дорожного полотна и почвы, град, метели и снежные заносы, речные заторы с наводнениями, ледяные обвалы и др. Природный лёд используется для хранения и охлаждения пищевых продуктов, биологических и медицинских препаратов, для чего он специально производится и заготавливается.
1.3 Выбор и обоснование опытов для проведения исследования
Для проведения опытов с водой необходимо выбрать те, которые наиболее полно характеризуют и подтверждают свойства воды.
Проведенный анализ показал, что лучше всего это будет реализовано при выполнении следующих опытов:
- Замерзание соленой воды.
- Расширение воды при замерзании.
- Замерзание жидкости при внешнем воздействии снега.
- Замерзание мыльных пузырей.
- Срастание сосульки.
- Скрип сухого снега.
- Примерзание к поверхности.
2. Проведение исследования
2.1 Подготовка материальной части
Для проведения опытов были взяты:
- предметы – кастрюля, стеклянная бутылка, пластиковая бутылка, одноразовые стаканы, тонкая медная проволока, трубочка;
- вещества – снег, сосулька, соль, вода, мыльный раствор, сок.
2.2 Проведение опытов с описанием основных результатов
1. Замерзание соленой воды.
Налейте в две формочки воду – чистую и очень солёную. Вынесите формочки на мороз или поставьте в морозильную камеру. Вы заметите, что чистая пресная вода превратилась в лёд, а солёная замёрзнет при очень сильном морозе.
Замерзание воды происходит не при температурных условиях ее наибольшей плотности (при 4 градусах Цельсия), а при нуле градусов Цельсия. Это свойства пресной воды.
При этом, морской лед отличается от пресноводного в ряде отношений. У соленой воды температура замерзания понижается по мере увеличения солености. В диапазоне солености от 30 до 35 промилле точка замерзания меняется от -1.6 до -1.9 град. Образование морского льда можно рассматривать как замерзание пресной воды с вытеснением солей в ячейки морской воды внутри толщи льда. Когда температура достигает точки замерзания, образуются ледяные кристаллы, которые «окружают» не замерзшую воду.
2. Расширение воды при замерзании.
Наполните водой пластиковый стакан, пластиковую бутылку и стеклянную бутылку. Выставьте их на мороз. Замерзая, вода увеличивается в объёме, «вылезает» из стакана, стеклянную бутылку разрывает даже в том случае, когда она заполнена наполовину. Пластиковая бутылка остаётся без видимых изменений.
При замерзании вода обладает уникальными свойствами расширения. Благодаря таким свойствам лед на воде, которая находится в виде жидкости, плавает.
Зимой из-за этого свойства воды происходят аварии на водопроводах. В сильные морозы основная причина таких аварий – замерзание текучей воды. Происходит ее расширение, так что образующийся лед легко разрывает трубы, так как плотность льда – 917 кг/м3, а плотность воды – 1000 кг/м3, то есть объем увеличивается в 1,1 раза, что довольно существенно.
3. Замерзание жидкости при внешнем воздействии снега.
Налейте в пластиковый стакан (пробирку) сок и поставьте его в кастрюлю с солёным снегом. Сок замёрзнет, и очень скоро вы будете лакомиться фруктовым льдом.
При смешивании соли со снегом наблюдается разрушение кристаллической структуры соли, которое происходит с поглощением тепла. Поэтому при смешивании снега с солью происходит активный отбор тепла из сока и сок превращается в лед.
4. Замерзание мыльных пузырей.
Приготовьте мыльный раствор. Раствор на морозе держите в рукавице, чтобы он не замёрз. Выдувайте пузыри трубочкой для сока. Из-за разности температур изнутри пузыря и снаружи возникает большая подъёмная сила, мгновенно уносящая пузыри вверх. Тонкая мыльная плёнка на морозе быстро замерзает, превращая пузыри в ледяные шарики.
Таким образом, тончайшая пленка мыльного пузыря замерзает за считанные секунды.
5. Срастание сосульки.
Возьмите сосульку. Перекиньте через неё тонкую проволоку, концы которой утяжелите грузиками. Наблюдайте, как проволока растапливает лёд, проникает всё глубже в сосульку. Вода над сосулькой вновь замерзает.
Это подтверждает свойство поглощения тепла большей массой льда.
Лед нарастает снизу, сразу над проволокой, так как стекающая вниз талая вода замерзает при соприкосновении с холодными стенками сосульки.
6. Скрип сухого снега.
Насыпьте в тарелку сахарный песок горкой и начните давить его ложкой. Вы услышите характерный скрип. Намочите песок и вновь разотрите. Скрип исчез. В морозные дни звук распространяется на большие расстояния.
Снег скрипит только в мороз (ниже -5°C), и звук скрипа меняется в зависимости от температуры воздуха – чем крепче мороз, тем выше тон скрипа. При достаточном опыте можно оценивать температуру воздуха по звуку, который издает скрипящий снег. Скрип образуется из-за того, что при давлении разрушаются мельчайшие кристаллики снега. Причем каждый из них по отдельности очень мал, чтобы издавать звук, доступный уху человека, но вместе они ломаются довольно громко. Усиление морозов делает ледяные кристаллики более твердыми и хрупкими. При каждом шаге ледяные иглы ломаются. При температуре воздуха ниже -50°C скрип снега становится таким сильным, что его можно слышать через тройные стекла (этому способствует также большая плотность морозного воздуха).
7. Примерзание к поверхности.
Добавьте в кастрюлю со снегом поваренную соль в соотношении примерно 1 к 6. Тщательно размешайте смесь. Если теперь вы захотите переставить кастрюлю, то её придётся поднять вместе с табуретом.
Это также подтверждает поглощение тепла из окружающей среды.
При смешивании соли со снегом происходит образование раствора, сопровождающееся сильным охлаждением вследствие большого поглощения теплоты льдом при его плавлении и солью при ее растворении. Так, например, температура смеси из 29 грамм соли и 100 грамм льда понижается до – 21°С. А если взять 143 грамма соли и 100 грамм льда, то температура может быть понижена до – 55°С.
2.3 Предложения по проведению опытов
Опыты по изучению свойств воды целесообразно проводить на уроках в средней и начальной школе.
При этом для детей начальной школы рекомендуется проведение опытов № 1 и 2 в домашних условиях под присмотром родителей.
Для учеников средней школы возможно проведение опытов № 3, 6 и 7 на уроках под руководством учителя, а опыты № 4 и 5 – факультативно или самостоятельно в домашних условиях.

Заключение
Таким образом, исследование свойств воды необходимо для человечества.
Процесс кристаллизации воды можно изучать в домашних условиях, а также на уроках в средней и начальной школе.
В работе удалось решить следующие задачи:
- Повести анализ основных свойств воды.
- Изучить значение кристаллизации воды для флоры и фауны Земли.
- Определить основные опыты для проведения исследования.
- Провести опыты и описать основные результаты.
- Подготовить предложения по проведению опытов на уроках в средней школе.
Значимость работы по систематизации основных свойств воды и значения кристаллизации воды для флоры и фауны Земли подтвердилась.
Источник