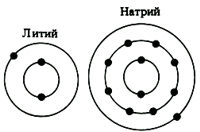
- Щелочные металлы
- I группа главная подгруппа Периодической системы Менделеева (щелочные металлы)
- Общая характеристика щелочных металлов
- Нахождение щелочных металлов в природе
- Способы получения щелочных металлов
- Химические свойства щелочных металлов
- Взаимодействие щелочных металлов с простыми веществами — неметаллами
- Взаимодействие щелочных металлов со сложными веществами
- Атомы элементов 1(Ia) группы
- Физические свойства щелочных металлов
- Химические свойства щелочных металлов
- Получение и применение щелочных металлов
Щелочные металлы
К щелочным металлам относят химические элементы: одновалентные металлы, составляющие Ia группу: литий, натрий, калий, рубидий, цезий и франций.
Эти металлы очень активны, быстро окисляются на воздухе и бурно реагируют с водой. Их хранят под слоем керосина из-за их сильной реакционной способности.
Общая характеристика
От Li к Fr (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств, реакционной способности. Уменьшается электроотрицательность, энергия ионизации, сродство к электрону.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 1 :
- Li — 2s 1
- Na — 3s 1
- K — 4s 1
- Rb — 5s 1
- Cs — 6s 1
- Fr — 7s 1
Природные соединения
В природе щелочные металлы встречаются в виде следующих соединений:
- NaCl — галит (каменная соль)
- KCl — сильвин
- NaCl*KCl — сильвинит
Получение
Получить такие активные металлы электролизом водного раствора — невозможно. Для их получения применяют электролиз расплавов при высоких температурах (естественно — безводных):
NaCl → Na + Cl2↑ (электролиз расплава каменной соли)
Химические свойства
Одной из особенностей щелочных металлов является их реакция с кислородом. Литий в такой реакции преимущественно образует оксид, натрий — пероксид, калий, рубидий и цезий — супероксиды.
K + O2 → KO2 (супероксид калия)
Реакции с неметаллами
Помните, что металлы никогда не принимают отрицательных степеней окисления. Щелочные металлы одновалентны, и проявляют постоянную степень окисления +1 в различных соединениях: гидриды, галогениды (фториды, хлориды, бромиды и йодиды), нитриды, сульфиды и т.д.
Li + H2 → LiH (в гидридах водород -1)
Na + F2 → NaF (в фторидах фтор -1)
Na + S → Na2S (в сульфидах сера -2)
K + N2 → K3N (в нитридах азот -3)
Реакция с водой
Щелочные металлы бурно взаимодействуют с водой, при этом часто происходит воспламенение, а иногда — взрыв.
Na + H2O → NaOH + H2↑ (воду можно представить в виде HOH — натрий вытесняет водород)
Иногда в задачах может проскользнуть фраза такого плана: «. в ходе реакции выделился металл, окрашивающий пламя горелки в желтый цвет». Тут вы сразу должны догадаться: речь, скорее всего, про натрий.
Щелочные металлы по-разному окрашивают пламя. Литий окрашивает в алый цвет, натрий — в желтый, калий — в фиолетовый, рубидий — синевато-красный, цезий — синий.
Оксиды щелочных металлов
Имеют общую формулу R2O, например: Na2O, K2O.
Получение
Получение оксидов щелочных металлов возможно в ходе реакции с кислородом. Для лития все совсем несложно:
В подобных реакциях у натрия и калия получается соответственно пероксид и супероксид, что приводит к затруднениям. Как из пероксида, так и из супероксида, при желании можно получить оксид:
Химические свойства
По свойствам эти оксиды являются основными. Они хорошо реагируют c водой, кислотными оксидами и кислотами:
Li2O + H2O → LiOH (осн. оксид + вода = основание — реакция идет, только если основание растворимо)
Na2O + SO2 → Na2SO3 (обратите внимание — мы сохраняем СО серы +4)
Гидроксиды щелочных металлов
Относятся к щелочам — растворимым основаниям. Наиболее известные представители: NaOH — едкий натр, KOH — едкое кали.
Получение
Гидроксиды щелочных металлов получаются в ходе электролиза водных растворов их солей, в реакциях обмена, в реакции щелочных металлов и их оксидов с водой:
KCl + H2O → (электролиз!) KOH + H2 + Cl2 (на катоде выделяется водород, на аноде — хлор)
Химические свойства
Проявляют основные свойства. Хорошо реагируют с кислотами, кислотными оксидами и солями, если в ходе реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).
LiOH + H2SO4 → LiHSO4 + H2O (соотношение 1:1, кислота в избытке — получается кислая соль)
2LiOH + H2SO4 → Li2SO4 + 2H2O (соотношение 2:1, основание в избытке — получается средняя соль)
KOH + SO2 → KHSO3 (соотношение 1:1 — получается кислая соль)
2KOH + SO2 → K2SO3 + H2O (соотношение 2:1 — получается средняя соль)
С амфотерными гидроксидами реакции протекают с образованием комплексных солей (в водном растворе) или с образованием окиселов — смешанных оксидов (при высоких температурах — прокаливании).
NaOH + Al(OH)3 → Na[Al(OH)4] (в водном растворе образуются комплексные соли)
NaOH + Al(OH)3 → NaAlO2 + H2O (при прокаливании образуется окисел — смесь двух оксидов: Al2O3 и Na2O, вода испаряется)
Реакции щелочей с галогенами заслуживают особого внимания. Без нагревания они идут по одной схеме, а при нагревании эта схема меняется:
NaOH + Cl2 → NaClO + NaCl + H2O (без нагревания хлор переходит в СО +1 и -1)
NaOH + Cl2 → NaClO3 + NaCl + H2O (с нагреванием хлор переходит в СО +5 и -1)
В реакциях щелочей с йодом образуется исключительно иодат, так как гипоиодит неустойчив даже при комнатной температуре, не говоря о нагревании. С серой реакция протекает схожим образом:
NaOH + I2 → NaIO3 + NaI + H2O (с нагреванием)
NaOH + S → Na2S + Na2SO3 + H2O (сера переходит в СО -2 и +4)
Уникальным является также взаимодействие щелочей с кислотным оксидом NO2, который соответствует сразу двум кислотам — и азотной, и азотистой.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
I группа главная подгруппа Периодической системы Менделеева (щелочные металлы)
I группа главная подгруппа Периодической системы Менделеева представляет собой щелочные металлы. К щелочным металлам относят химические элементы:
Литий Li,
Натрий Na,
Калий K,
Цезий Cs,
Рубидий Rb
Франций Fr
Эти металлы очень активны, поэтому их хранят под слоем вазелина или керосина.
Общая характеристика щелочных металлов
От Li к Fr (сверху вниз в периодической таблице) происходит увеличение:
- атомного радиуса,
- металлических, основных, восстановительных свойств,
- реакционной способности.
Уменьшается
- электроотрицательность,
- энергия ионизация,
- сродство к электрону.
Электронные конфигурации у данных элементов схожи, все они содержат 1 электрон на внешнем уровне ns 1 :
Следовательно, типичная степень окисления щелочных металлов в соединениях +1.
Нахождение щелочных металлов в природе
Способы получения щелочных металлов
Литий
- Литий получают в промышленности электролизом расплавахлорида лития в смеси с KCl или BaCl2 (эти соли служат для понижения температуры плавления смеси):
- Известен также способ получения лития из его оксида в вакууме при 300°С:
Натрий
- Натрий получают электролизом расплава хлорида натрия с добавками хлорида кальция:
2NaCl (расплав) → 2Na + Cl2
Электролитом обычно служит смесь NaCl с NaF и КСl (что позволяет проводить процесс при 610–650°С).
- Натрий можно получить, прокаливая соду с углем в закрытых тиглях, пары металла конденсируются на крышке тигля, выход реакции невысокий:
Калий
- Калий получают также электролизом расплавов солей или расплава гидроксида калия, однако на практике таким способом их не получают из-за высокой химической активности
- Наиболее распространены методы термохимического восстановления: восстановление калия из расплавов хлоридов или гидроксидов.:
KCl + Na = K + NaCl
KOH + Na = K + NaOH
В качестве восстановителей используют пары натрия, карбид кальция, алюминий, кремний
Цезий, Рубидий
- Цезий и рубидий получают восстановлением их хлоридов специально подготовленным кальцием при 700–800 °С:
Са + 2CsCl → 2Cs + CaCl2
- В качестве восстановителя также используют цирконий, реакция протекает при 650 °С:
- В промышленности используют преимущественно физико-химические методы выделения чистого цезия: многократную ректификацию в вакууме
Химические свойства щелочных металлов
Качественные реакции — окрашивание пламени солями щелочных металлов
Цвет пламени:
Li — карминно-красный
Na — желтый
K — фиолетовый
Rb — буро-красный
Cs — фиолетово-красный
Взаимодействие щелочных металлов с простыми веществами — неметаллами
С кислородом
- Литий образует оксид:
- Натрий образует пероксид:
- Калий образует надпероксид:
С галогенами (F, Cl, Br, I)
Щелочные металлы образуют галогениды:
С водородом
Щелочные металлы образуют гидриды:
С серой
Щелочные металлы образуют сульфиды:
С азотом
При комнатной температуре взаимодействует только литий:
Остальные щелочные металлы реагируют с азотом при нагревании:
С углеродом
Щелочные металлы при нагревании образуют карбиды, преимущественно ацетилениды:
С фосфором
Щелочные металлы активно реагируют с фосфором образуя фосфиды:
Взаимодействие щелочных металлов со сложными веществами
С водой
Щелочные металлы реагируют с водой при обычных условиях:
С кислотами
- С растворами HCl, H2SO4щелочные металлы взаимодействуют с образованием соли и выделением водорода:
с концентрированной серной:
с разбавленной азотной
с концентрированной азотной
- Со слабыми кислотами
С солями
В расплаве щелочные металлы могут взаимодействовать с некоторыми солями:
3Na + AlCl3 → 3NaCl + Al
Запомните! В растворе щелочные металлы взаимодействуют с водой, а не с солями других металлов.
Источник
Атомы элементов 1(Ia) группы
| Элемент | Li | Na | K | Rb | Cs | Fr |
|---|---|---|---|---|---|---|
| Порядковый номер | 3 | 11 | 19 | 37 | 55 | 87 |
| Атомная масса (относительная) | 6,94 | 22,98 | 39,09 | 85,46 | 132,9 | 223 |
| Плотность (н.у.), г/см 3 | 0,534 | 0,971 | 0,856 | 1,53 | 1,87 | 1,87 |
| tпл, °C | 180 | 97 | 63 | 39 | 28 | 18 |
| tкип, °C | 1339 | 882 | 773 | 668 | 667 | 640 |
| Энергия ионизации, кДж/моль | 513,3 | 495,8 | 418,8 | 403,0 | 375,7 | 380 |
| Электронная формула | [He]2s 1 | [Ne]3s 1 | [Ar]4s 1 | [Kr]5s 1 | [Xe]6s 1 | [Rn]7s 1 |
| Электроотрицательность (по Поллингу) | 0,98 | 0,93 | 0,82 | 0,82 | 0,79 | 0,7 |
Электронные формулы инертных газов:
- He — 1s 2 ;
- Ne — 1s 2 2s 2 2p 6 ;
- Ar — 1s 2 2s 2 2p 6 3s 2 3p 6 ;
- Kr — [Ar]3d 10 4s 2 4p 6 ;
- Xe — [Kr]4d 10 5s 2 5p 6 ;
- Rn — [Xe]4f 14 5d 10 6s 2 6p 6 .
Соединения щелочных металлов:
В 1 группу(Ia группу по старой классификации) периодической таблицы химических элементов Д. И. Менделеева входят 6 металлов: литий, натрий, калий, рубидий, цезий, франций (см. таблицу выше). Эти металлы принято называть щелочными, поскольку при взаимодействии с водой эти металлы (и их оксиды) образуют щелочи.
Самым распространенным из щелочных металлов в земной коре является натрий (2,3% по массе), далее идут калий (2,1%), рубидий (0,009%), литий (0,002%), цезий (0,0003%). Щелочные металлы по причине их высокой активности в природе в свободном виде не встречаются.
Природные соединения и минералы, богатые натрием и калием:
Все атомы элементов 1(Ia) группы на внешнем энергетическом уровне имеют по одному валентному s-электрону (см. Электронная конфигурация атомов), с которым в химических соединениях достаточно легко «расстаются» с целью завершения внешнего энергетического уровня, который становится в таком случае устойчивым, по аналогии с завершенным энергетическим уровнем инертных газов.
Таким образом, отдавая «ненужный» электрон щелочные металлы в химических соединениях проявляют степень окисления +1.
Нетрудно заметить, что с ростом порядкового номера щелочного металла увеличивается не только общее кол-во электронов (энергетических уровней), но также и радиус атома, что в свою очередь, обуславливает уменьшение энергии ионизации (соответственно усиление металлических свойств элемента) в направлении от лития к францию (по мере увеличения радиуса атома щелочного элемента) — франций со своим s-электроном расстается гораздо легче, чем литий. Говоря другими словами, с ростом радиуса атома (номера элемента) возрастает реакционная (восстановительная) способность щелочного металла.
Физические свойства щелочных металлов
Многие физические свойства щелочных металлов обусловлены металлическими связями, возникающими между атомами этих металлов по причине их низкой энергии ионизации:
- щелочные металлы имеют серебристо-белый цвет;
- низкую плотность;
- низкую температуру плавления (температуры плавления уменьшаются в подгруппе сверху-вниз);
- обладают высокой пластичностью;
- высокой электро- и теплопроводностью.
Химические свойства щелочных металлов
Как уже было сказано выше, щелочные металлы очень легко вступают в химические реакции с другими элементами, отдавая при этом «ненужный» валентный электрон (см. Валентность) и превращаясь в положительно заряженный ион (катион).
Щелочные металлы легко реагируют со многими простыми веществами:
- с кислородом щелочные металлы образуют оксиды (Li), пероксиды (Na), суперпероксиды:
4Li + O2 = 2Li2O; 2Na + O2 = Na2O2; K + O2 = KO2; - с серой образуют сульфиды:
2Na+S = Na2S - с водородом образуют гидриды:
2Na+H2 = 2NaH - взаимодействуют с галогенами (F, Cl, Br, I), образуя галогениды:
2Li + F2 = 2LiF; - бурно реагируют с водой (активность возрастает с ростом атомного номера — натрий воспламеняется, а рубидий взрывается):
2Na + 2H2O = 2NaOH + H2; - бурно реагируют с кислотами:
- с соляной и разбавленной серной реагируют с выделением водорода:
2K + H2SO4(рзб) = K2SO4 + H2; - с концентрированной серной восстанавливают серу до степени окисления -2:
8Na + 5H2SO4(кнц) = 4Na2SO4 + H2S + 4H2O; - с разбавленной азотной продуктом восстановления является нитрат аммония (ст. ок. -4) или аммиак:
8Na + 10HNO3(рзб) = 8NaNO3 + NH4NO3 + 3H2O; - с концентрированной азотной продуктом восстановления является оксид азота (I):
8Na + 10HNO3(кнц) = 8NaNO3 + N2O + 5H2O.
- с соляной и разбавленной серной реагируют с выделением водорода:
Щелочные металлы окрашивают пламя в следующие цвета:
- Li — светло-красный;
- Na — желтый;
- K — сине-фиолетовый;
- Rb — темно-красный;
- Cs — бледно-голубой.
Получение и применение щелочных металлов
Промышленным способом щелочные металлы получают электролизом расплавов хлоридов (гидроксидов) этих металлов.
Металлотермические методы получения щелочных металлов (рубидий и цезий получают в вакуумной среде):
- 3LiO + 2Al = Al2O3 + 3Li;
- Na + KCl = NaCl + K;
- 2RbCl + Ca = 2Rb + CaCl2;
- 2CsCl + Mg = 2Cs + MgCl2.
Применение щелочных металлов:
- Li:
- придает легкость сплавам, его применяют при производстве медных, магниевых и алюминиевых сплавов;
- в металлургии при помощи лития удаляют из металлических расплавов шлаки, содержащие азот, кислород и серу;
- в органическом синтезе.
- Na:
- в качестве наполнителей газоразрядных ламп;
- в качестве теплоносителя в ядерных реакторах;
- в органическом и неорганическом синтезе;
- в металлургии при производстве металлов и сплавов.
- K:
- для получения металлов;
- в качестве теплоносителя в ядерных реакторах;
- в фотоэлементах в качестве преобразователя световой энергии в электрическую.
- Rb, Cs:
- в источниках инфракрасного излучения;
- в фотоэлементах.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Источник