- Практ. 1
- Практическая работа № 2 Получение этилена и изучение его свойств.
- Дистанционное обучение как современный формат преподавания
- Современные педтехнологии в деятельности учителя
- Современные образовательные технологии в преподавании химии с учетом ФГОС
- Оставьте свой комментарий
- Подарочные сертификаты
- Получение этилена и исследование его свойств. Подготовка к уроку
- Просмотр содержимого документа «инструкция практическая работа»
- Просмотр содержимого документа «маршрутный лист»
- Взаимодействие этилена с йодной водой срочно надо?
- Продуктом взаимодействия этилена с водой является?
- ОТЛИЧИТЬ ПРОПАН ОТ ПРОПИНА МОЖНО С ПОМОЩЬЮ : А) раствора щелочи ; Б) раствора кислоты ; В) раствора перманганата калия ; Г) йодной воды?
- Взаимодействие этилена с раствором перманганата калия C2H4 + KMnO4 — > ; ?
- Вычислите количества вещества этилена, при взаимодействий которого с хлором образуется 9, 9гр дихлорэтана?
- Взаимодействие этилена с раствором перманганата калия?
- Срочно?
- Свойства как метана, так и этилена характеризуют следующее :а) могут взаимодействовать с кислородомб) обесцвечивают бромную водув) являются газообразными веществами, хорошо растворимыми в водеда)взаим?
- Сколько граммов этанола получится при взаимодействии 280 граммов этилена с водой, если выход этилена составляет 50%?
- Масса этанола который образуется при взаимодействии 2, 8г этилена и 36г воды?
- Что будет наблюдаться, если этилен пропустить череза) бромную водуб) раствор перманганата калия (KMnO4)?
Практ. 1
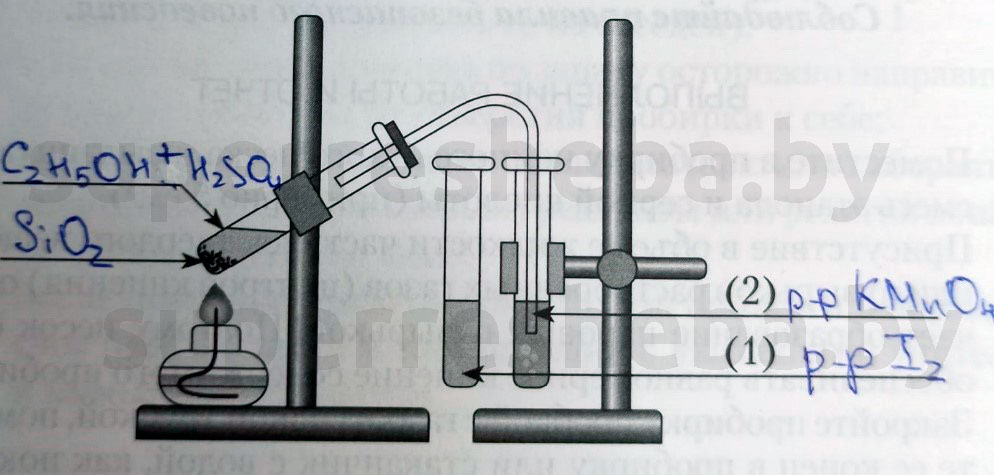
Напишите над стрелками формулы или названия веществ в пробирках.
Объясните явления, которые наблюдаются в процессе получения этилена.
В процессе получения мы наблюдали появление пузырьков газа и обесцвечивание растворов иода и перманганата калия. (Причины обесцвечивания приведены далее).
Приведите уравнение реакции получения этилена.
+ ° C 2 H 4 ↑ + H 2 O .
Объясните явления, наблюдаемые при пропускании этилена в пробирки с растворами иода (1) и перманганата калия (2).
В процессе получения этилена мы наблюдали обесцвечивание растворов иода и перманганата калия, потому что образовывались бесцветные продукты реакции. Раствор перманганата обесцвечивался, т.к. в ходе реакции перманганат переходил в щелочь и оксид марганца (IV), а раствора иода – потому что молекулы иода встраивались в молекулу этилена.
Приведите уравнения реакции этилена с раствором иода.
Приведите схему реакции этилена с раствором K M n O 4 \mathrm
Приведите уравнение реакции горения этилена.
1. Напишите, благодаря наличию какого структурного фрагмента в молекулах алкенов они вступают в реакции с иодной и бромной водой. К какому типу относятся данные реакции?
Алкены вступают в реакции с иодной и бромной водой благодаря наличию двойной связи. Эти реакции относятся к реакциям присоединения.
2. В каких условиях реагируют с бромом алканы? К какому типу относится реакция алканов с бромом?
Алканы реагируют с бромом на свету. Это реакция замещения.
3. Сравните отношение к бромной воде алканов и алкенов. Можно ли различить этан и этен при помощи бромной воды?
Да, можно. При пропускании этана через бромную воду раствор брома не будет обесцвечиваться, а при пропускании этена — будет.
Источник
Практическая работа № 2 Получение этилена и изучение его свойств.
Нечаев Дмитрий Валерьевич, учитель химии
ГУ ЛНР «ЛУВК « ИНТЕЛЛЕКТ»
Практическая работа № 2
Получение этилена и изучение его свойств.
Цель: научиться получать в лаборатории этилен; изучить физические и химические свойства этилена.
Оборудование: пробирки, пробка с газоотводной трубкой, штатив, спиртовая горелка, спички.
С правилами техники безопасности ознакомлен(а) и обязуюсь их выполнять.
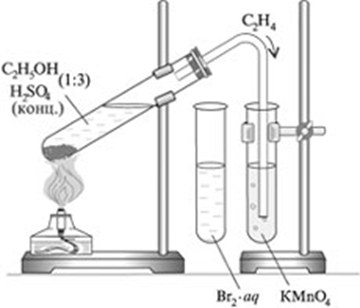
В пробирку налили 1 мл этилового спирта и осторожно добавьте 6—9 мл концентрированной серной кислоты. Затем всыпали немного прокаленного песка (чтобы предотвратить толчки жидкости при кипении). Закрыли пробирку пробкой с газоотводной трубкой, закрепили ее в штативе и осторожно нагрели содержимое пробирки.
В пробирке начинается выделяться газ — этилен.
В ходе реакции концентрированная серная кислота забирает воду из спирта, врезультате образуется этилен.
Такую реакцию называют – реакция дегидратации.
Изучение свойств этилена.
В другую пробирку налили 2-3 мл бромной воды. Опустили газоотводную трубку первой пробирки до дна пробирки с бромной водой и пропускали через неё выдедяющийся газ.
При пропускании газа через бромную воду, происходит обесцвечивание бромной воды.
В ходе реакции происходит окисление этилена бромной водой по двойной связи.
В третью пробирку налили 2-3 мл разбавленного раствора KMnO 4 , поодкисленного серной кислотой, и пропустили через него газ.
При пропускании газа через подкисленный раствор KMnO4 , происходит обесцвечивание раствора KMnO 4 .
В ходе реакции происходит окисление этилена подкисленным раствором перманганата калия.
Выделяющиеся газ первой пробирки подожгли.
Этилен на воздухе горит ярким светящимся пламенем.
Этилен горит ярким светящимся пламенем, что доказывает наличие кратных связей.
Общий вывод: на данной практической работе мы научились получать в лаборатории этилен реакцией дегидратации спиртов; изучили химические свойства этилена, а именно, действие этилена на бромную воду и подкисленный раствор перманганата калия.
Какой из гомологов этена имеет плотность по воздуху 1,45?
Ответ: D (возд.) = Mr ( алкена)/Mr (воздуха);
Mr ( алкена) = D (возд.)* Mr (воздуха);
Mr ( алкена) = 1,45*29 = 42.
Какой из гомологов пропена имеет плотность по водороду 14?
Ответ: D (Н2) = Mr ( алкена)/Mr (Н 2 );
Mr ( алкена) = 14*2 = 28.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс повышения квалификации
Современные педтехнологии в деятельности учителя
Курс повышения квалификации
Современные образовательные технологии в преподавании химии с учетом ФГОС
Номер материала: ДБ-1175165
Международная дистанционная олимпиада Осень 2021
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
В России появился стандарт сбора цифрового следа в образовании
Время чтения: 2 минуты
В России создали сообщество активных родителей
Время чтения: 2 минуты
Рособрнадзор оставил за регионами решение о дополнительных школьных каникулах
Время чтения: 1 минута
Основы православной культуры чаще всего преподают учителя начальных классов
Время чтения: 2 минуты
В России объявлены нерабочие дни с 30 октября по 7 ноября
Время чтения: 2 минуты
В школе в Пермском крае произошла стрельба
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Источник
Получение этилена и исследование его свойств. Подготовка к уроку

Просмотр содержимого документа
«инструкция практическая работа»
Практическая работа №2
«Получение этилена и изучение его свойств».
Уравнения реакции и выводы
Рассмотрите и соберите прибор как показано на рисунке, проверьте его на герметичность.
Отмерьте мерным цилиндром 1мл этилового спирта и перелейте в пробирку, затем осторожно добавьте 3 мл концентрированной серной кислоты.
Поместите в смесь немного предварительно прокаленного песка (или кусочек пемзы), чтобы избежать толчков жидкости при кипении
Закройте пробирку пробкой с газоотводной трубкой и укрепите в штативе. Конец газоотводной трубки опустите в пробирку с йодной водой (бромной водой).
Осторожно нагревайте смесь!
Изучение свойств этилена
Опишите физические свойства этилена:
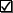
Опыт 2. Взаимодействие этилена с йодной (бромной) водой
• Пропускайте этилен через 1-2 мл йодной (бромной) воды.
• Следите, чтобы нагревание смеси не прекращалось. Не допускайте переброс жидкости из пробирки в прибор.
• Какие изменения происходят с йодной (бромной) водой? Объясните наблюдаемое явление.
Опыт 3. Взаимодействие этилена с раствором перманганата калия
• Пропускайте газ через 1-2 мл раствора перманганата калия.
• Объясните, что наблюдаете?
Опыт 4. Горение этилена на воздухе
• Выньте газоотводную трубку из раствора, и повернув её отверстием к верху, подожгите выделяющийся газ.
• Каким (светящимся или несветящимся) пламенем горит этилен? Дайте объяснение.
• Потушите спиртовку. Выделение этилена постепенно прекратится.
Определите молекулярную формулу этиленового углеводорода, молекулярная масса которого 96?
Сделайте общий вывод о проделанной работе, исходя из цели
Просмотр содержимого документа
«маршрутный лист»
Предлагаю выполнить вам тренировочное упражнение
«Непредельные углеводороды — Алкены»
и упражнение контрольного характера «контрольные задания В1».
Можете начать работу с любого упражнения.
Инструкция для работы в лаборатории «Он-лайн работа»
Пройди по ссылке в РЭШ, выполни тест и оцени свои знания.
Пройди по ссылке в РЭШ, выполни тренировочные упражнения и виртуальную лабораторную работу, проверь результаты и запиши в маршрутный лист.
Инструкция для работы в лаборатории «Практическая работа»
Повторите правила техники безопасности и оцените свои знания.
Оценку запиши в маршрутный лист
Выполни практическую работу, заполни форму отчета.
Следи за порядком на своем рабочем месте
Сдай отчет учителю
В лаборатории «Он-лайн работа» пройди по ссылке и оцени свою работу на уроке.
Источник
Взаимодействие этилена с йодной водой срочно надо?
Химия | 10 — 11 классы
Взаимодействие этилена с йодной водой срочно надо.
Образование 2 — йодоэтилена.
После 2 — дийодоэтилена.
Далее закрывается 1 молекула.
1 — моно, 2 — диийодоэтилен.
1, 2 — дийодоэтилен.
При этом разрушается двойная связь.
Продуктом взаимодействия этилена с водой является?
Продуктом взаимодействия этилена с водой является.
ОТЛИЧИТЬ ПРОПАН ОТ ПРОПИНА МОЖНО С ПОМОЩЬЮ : А) раствора щелочи ; Б) раствора кислоты ; В) раствора перманганата калия ; Г) йодной воды?
ОТЛИЧИТЬ ПРОПАН ОТ ПРОПИНА МОЖНО С ПОМОЩЬЮ : А) раствора щелочи ; Б) раствора кислоты ; В) раствора перманганата калия ; Г) йодной воды.
Взаимодействие этилена с раствором перманганата калия C2H4 + KMnO4 — > ; ?
Взаимодействие этилена с раствором перманганата калия C2H4 + KMnO4 — > ; .
Вычислите количества вещества этилена, при взаимодействий которого с хлором образуется 9, 9гр дихлорэтана?
Вычислите количества вещества этилена, при взаимодействий которого с хлором образуется 9, 9гр дихлорэтана.
Взаимодействие этилена с раствором перманганата калия?
Взаимодействие этилена с раствором перманганата калия.
Срочно?
Вычислите объем водорода, полученного при взаимодействии 4, 6г натрия с водой.
Свойства как метана, так и этилена характеризуют следующее :а) могут взаимодействовать с кислородомб) обесцвечивают бромную водув) являются газообразными веществами, хорошо растворимыми в водеда)взаим?
Свойства как метана, так и этилена характеризуют следующее :
а) могут взаимодействовать с кислородом
б) обесцвечивают бромную воду
в) являются газообразными веществами, хорошо растворимыми в воде
да)взаимодействуют с бромоводородом.
Сколько граммов этанола получится при взаимодействии 280 граммов этилена с водой, если выход этилена составляет 50%?
Сколько граммов этанола получится при взаимодействии 280 граммов этилена с водой, если выход этилена составляет 50%?
Масса этанола который образуется при взаимодействии 2, 8г этилена и 36г воды?
Масса этанола который образуется при взаимодействии 2, 8г этилена и 36г воды.
Что будет наблюдаться, если этилен пропустить череза) бромную водуб) раствор перманганата калия (KMnO4)?
Что будет наблюдаться, если этилен пропустить через
б) раствор перманганата калия (KMnO4)?
И то произойдет, если этилен заменить метаном?
На этой странице сайта размещен вопрос Взаимодействие этилена с йодной водой срочно надо? из категории Химия с правильным ответом на него. Уровень сложности вопроса соответствует знаниям учеников 10 — 11 классов. Здесь же находятся ответы по заданному поиску, которые вы найдете с помощью автоматической системы. Одновременно с ответом на ваш вопрос показаны другие, похожие варианты по заданной теме. На этой странице можно обсудить все варианты ответов с другими пользователями сайта и получить от них наиболее полную подсказку.
Что — то напутанно в условии у вас. Система не решается.
Источник