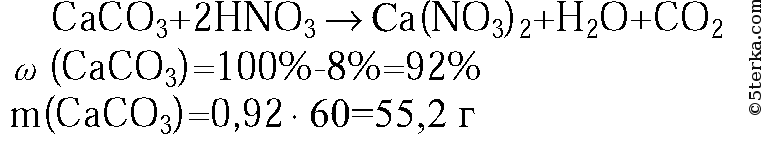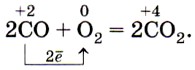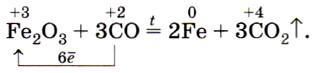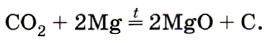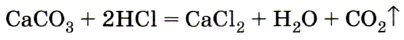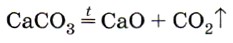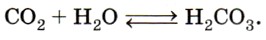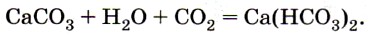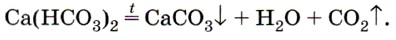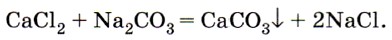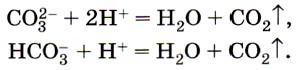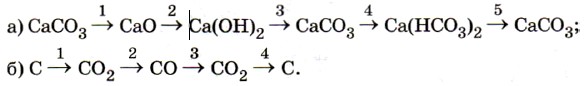Вариант 2
Вопросы:
1. В виде каких простых веществ углерод встречается в природе? Сравните их физические свойства. Объясните зависимость физических свойств от структуры кристаллической решетки.
2. Напишите уравнения реакций: а) оксида углерода(IV) с известковой водой; б) углерода с водородом; в) горения углерода в избытке кислорода.
3. Какой объем воздуха (н. у.) расходуется при полном сгорании 84 л оксида углерода(II)? Объемная доля кислорода в воздухе составляет 21 %. (Ответ: 200 л.)
Ответы и решения:
1. Углерод в природе встречается в виде:
а) алмаза — очень твердое, прочное вещество с высокой tпл, кристаллическая решетка — атомная.
б) графита — твердое вещество, жирное на ощупь с высокой tпл электро- и теплопроводен, кристаллическая решетка атомная.
в) карбина — твердое вещество (тверже графита, но мягче алмаза), черный мелкокристаллический порошок, обладает полупроводниковыми свойствами. Кристаллическая решетка атомная.

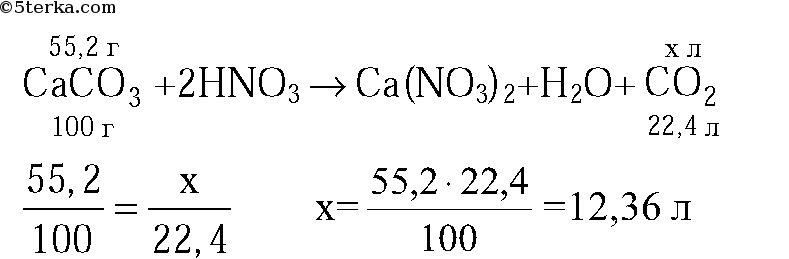


задача №2
к главе «Тема IV. Подгруппа углерода. Работа 1. Углерод. Оксиды углерода».
Источник
Взаимодействие оксида углерода с известковой водой при
- Текст, выделенный СИНИМ ШРИФТОМ обязателен для конспектирования.
- В тексте есть ссылки на видеофрагменты, обязательно посмотрите их!
Оксид углерода (II) – СО ( угарный газ , окись углерода , монооксид углерода )
Физические свойства: бесцветный ядовитый газ без вкуса и запаха, горит голубоватым пламенем, легче воздуха, плохо растворим в воде. Концентрация угарного газа в воздухе 12,5—74 % взрывоопасна.
Формальная степень окисления углерода +2 не отражает строение молекулы СО, в которой помимо двойной связи, образованной обобществлением электронов С и О, имеется дополнительная, образованная по донорно-акцепторному механизму за счет неподеленной пары электронов кислорода:
В связи с этим молекула СО очень прочна и способна вступать в реакции окисления-восстановления только при высоких температурах. При обычных условиях СО не взаимодействует с водой, щелочами или кислотами.
Основным антропогенным источником угарного газа CO в настоящее время служат выхлопные газы двигателей внутреннего сгорания. Угарный газ образуется при сгорании топлива в двигателях внутреннего сгорания при недостаточных температурах или плохой настройке системы подачи воздуха (подается недостаточное количество кислорода для окисления угарного газа CO в углекислый газ CO2). В естественных условиях, на поверхности Земли, угарный газ CO образуется при неполном анаэробном разложении органических соединений и при сгорании биомассы, в основном в ходе лесных и степных пожаров.
1) Получение в промышленности (в газогенераторах):
CO2 + C = 2CO – 175 кДж
В газогенераторах иногда через раскалённый уголь продувают водяной пар:
смесь СО + Н2 – называется синтез – газом .
2) Получение СО в лаборатории — термическим разложением муравьиной или щавелевой кислоты в присутствии H2SO4(конц.):
При обычных условиях CO инертен; при нагревании – восстановитель ;
Характер свойств угарного газа CO — несолеобразующий оксид.
1) Взаимодействие с кислородом:
2 C +2 O + O 2 t ˚ C → 2 C +4 O 2 ↑
C +2 O + CuO t ˚ C → Сu + C +4 O2↑
3) Взаимодействие с хлором (на свету)
CO + Cl2 свет → COCl2 (фосген – ядовитый газ)
4) Взаимодействие с расплавами щелочей (под давлением)
CO + NaOH P асплав → HCOONa (формиат натрия)
Влияние угарного газа на живые организмы:
Угарный газ опасен, потому что он лишает возможности кровь нести кислород к жизненно важным органам, таким как сердце и мозг. Угарный газ объединяется с гемоглобином, который переносит кислород к клеткам организма, в следствии чего тот становится непригодным для транспортировки кислорода. В зависимости от вдыхаемого количества, угарный газ ухудшает координацию, обостряет сердечно-сосудистые заболевания и вызывает усталость, головную боль, слабость, Влияние угарного газа на здоровье человека зависит от его концентрации и времени воздействия на организм. Концентрация угарного газа в воздухе более 0,1% приводит к смерти в течение одного часа, а концентрация более 1,2% в течении трех минут.
Применение оксида углерода :
Главным образом угарный газ применяют, как горючий газ в смеси с азотом, так называемый генераторный или воздушный газ, или же в смеси с водородом водяной газ. В металлургии для восстановления металлов из их руд. Для получения металлов высокой чистоты при разложении карбонилов.
Оксид углерода (IV) СO2 – углекислый газ
Физические свойства: Углекислый газ, бесцветный, без запаха, растворимость в воде — в 1V H2O растворяется 0,9V CO2 (при нормальных условиях); тяжелее воздуха; t°пл.= -78,5°C (твёрдый CO2 называется «сухой лёд»); не поддерживает горение и дыхание.
Строение молекулы: Углекислый газ имеет следующие электронную и структурную формулы —
Все четыре связи ковалентые полярные.
Получение углекислого газа:
1. В промышленности: Термическим разложением солей угольной кислоты (карбонатов). Обжиг известняка.
2. В лаборатории. Действием сильных кислот на карбонаты и гидрокарбонаты –
3. Сгорание углеродсодержащих веществ:
4. При медленном окислении в биохимических процессах (дыхание, гниение, брожение)
Характер свойств углекислого газа — это Кислотный оксид:
1) Взаимодействие с водой с образованием непрочной угольной кислоты:
2) Взаимодействие с основными оксидами и основаниями, образуя соли угольной кислоты — карбонаты
Качественная реакция на углекислый газ: п омутнение известковой воды Ca ( OH )2 за счёт образования белого осадка – нерастворимой соли CaCO 3 :
Источник
9 класс. Химия. Неорганические соединения углерода
9 класс. Химия. Неорганические соединения углерода
Вопросы
Задай свой вопрос по этому материалу!
Поделись с друзьями
Комментарии преподавателя
Оксид углерода (II), или, как его еще можно назвать, монооксид углерода, а также угарный газ – это несолеобразующий оксид. По своим физическим свойствам оксид углерода (II) – бесцветный газ, без запаха, плохо растворимый в воде. Угарным газом это вещество называют потому, что оно очень ядовито.
Монооксид углерода образуется при неполном сгорании угля или органических веществ:
В лаборатории его легче всего получить, действуя на муравьиную кислоту концентрированной серной кислотой, которая связывает воду:
Оксид углерода (II) – сильный восстановитель, его широко используют в металлургии для восстановления металлов из их оксидов:
СО + CuO = Cu + CO2
В кислороде и на воздухе оксид углерода (II) горит голубоватым пламенем, выделяя много теплоты, при этом образуется оксид углерода (IV):
2СО + О2 = 2СО2 + 577 кДж
Оксид углерода (IV), или диоксид углерода, а также углекислый газ является типично кислотным оксидом, в котором углерод находится в степени окисления +4. Этот оксид способен взаимодействовать с водой с образованием угольной кислоты, с основными оксидами и щелочами.
Углекислый газ не имеет цвета и запаха, в 1,5 раза тяжелее воздуха и неплохо растворим в воде. Всем известная газированная вода – это раствор оксида углерода (IV) в воде. При обычной температуре и высоком давлении диоксид углерода сжижается. При его испарении поглощается так много теплоты, что часть оксида углерода (IV)превращается в снегообразную массу – «сухой лед» (Рис. 1).
Рис. 1. Сухой лед
Благодаря тому, что оксид углерода (IV) не поддерживает горения, им заполняют огнетушители.
При растворении оксида углерода (IV) в воде образуется угольная кислота:
СО2 + Н2О ↔ Н2СО3
Эта кислота относится к слабым кислотам и в водном растворе подвергается ступенчатой диссоциации:
Для угольной кислоты характерно образование кислых солей.
ОПЫТ 1. Пропустим через раствор гидроксида кальция углекислый газ, получаем нерастворимый карбонат кальция (Рис. 2).
Ca(OH)2 + CO2 = CaCO3 ↓ + H2O
Рис. 2. Карбонат кальция
Карбонаты – соли угольной кислоты, в которых замещены оба иона водорода. Когда замещен только один ион водорода, получаются гидрокарбонаты. Большинство карбонатов – нерастворимые соединения, все гидрокарбонаты – растворимые. Нерастворимый карбонат превращается в растворимый гидрокарбонат при пропускании через раствор с осадком углекислого газа.
CaCO3 + CO2 + H2O ↔ Ca(HCO3)2
При нагревании раствора гидрокарбоната выделяется углекислый газ, и вновь образуется нерастворимый карбонат кальция.
Ca(HCO3)2 = CaCO3↓ + CO2 + H2O
Разложение гидрокарбонатов при небольшом нагревании нашло свое применение. Например, гидрокарбонат натрия (в быту он называется пищевой содой) начинает разлагаться уже при 50°С:
2NaHCO3 = Na2CO3 + H2O + CO2↑
Пищевую соду используют, например, при выпечке хлеба. При нагревании она разлагается с образованием диоксида углерода, благодаря чему хлеб становится пышным.
Для всех солей угольной кислоты характерна обменная реакция с кислотами, признаком которой является выделение углекислого газа, так как в результате этой реакции образуется угольная кислота, которая сразу разлагается на воду и углекислый газ. Например, при взаимодействии карбоната кальция с соляной кислотой образуются хлорид кальция, вода и углекислый газ:
Источник
§ 34. Кислородные соединения углерода
Углерод образует два оксида — оксид углерода (II) СО и оксид углерода (IV) CO2.
Оксид углерода (II) СО — бесцветный, не имеющий запаха газ, малорастворимый в воде. Его называют угарным газом, так как он очень ядовит. Попадая при дыхании в кровь, он быстро соединяется с гемоглобином, образуя прочное соединение карбоксигемоглобин (объясните происхождение этого термина), тем самым лишая гемоглобин возможности переносить кислород. При вдыхании воздуха, содержащего 0,1% СО, человек может внезапно потерять сознание и умереть. Угарный газ образуется при неполном сгорании топлива (напишите уравнение соответствующей химической реакции), вот почему так опасно преждевременное закрывание дымоходов печей (рис. 152).
Оксид углерода (II) относят, как вы уже знаете, к несолеобразующим оксидам. Будучи оксидом неметалла, он должен реагировать с щелочами и основными оксидами с образованием соли и воды, однако этого не наблюдается.
Оксид углерода (II) способен отнимать кислород у оксидов металлов, т. е. восстанавливать металлы из их оксидов:
Именно это свойство оксида углерода (II) используют в металлургии при выплавке чугуна.
Оксид углерода (IV) СO2 — бесцветный, не имеющий запаха газ, широко известный под названием углекислый газ. Он примерно в полтора раза тяжелее воздуха. При обычных условиях в одном объёме воды растворяется один объём углекислого газа.
При давлении примерно 60 атм углекислый газ превращается в бесцветную жидкость. При испарении жидкого углекислого газа часть его превращается в твёрдую снегообразную массу, которую в промышленности прессуют, — это известный вам «сухой лёд», который применяют для хранения пищевых продуктов. Вы уже знаете, что твёрдый углекислый газ имеет молекулярную решётку и способен к возгонке (что это такое?).
Углекислый газ СO2 как типичный кислотный оксид взаимодействует с щелочами (например, вызывает помутнение известковой воды), с основными оксидами и водой. Он не горит и не поддерживает горения (рис. 153) и потому применяется для тушения пожаров. Однако магний продолжает гореть в углекислом газе с образованием оксида и выделением углерода в виде сажи:
Углекислый газ получают, действуя на соли угольной кислоты — карбонаты растворами соляной, азотной и даже уксусной кислот. В лаборатории углекислый газ получают при действии соляной кислоты на мел или мрамор (рис. 154):
В промышленности углекислый газ получают обжигом известняка:
Углекислый газ используют также для изготовления шипучих напитков и получения соды.
Применение углекислого газа показано на рисунке 155.
При растворении оксида углерода (IV) в воде образуется очень нестойкая угольная кислота Н2СO3, которая легко разлагается на исходные компоненты — углекислый газ и воду:
Будучи двухосновной, угольная кислота образует два ряда солей: средние — карбонаты, например СаСO3, и кислые — гидрокарбонаты, например Са(НСO3)2. Из карбонатов в воде растворимы только соли калия, натрия и аммония. Кислые соли, как правило, растворимы в воде.
При избытке углекислого газа в присутствии воды карбонаты могут превращаться в гидрокарбонаты. Так, если через известковую воду пропускать углекислый газ, то она сначала помутнеет из-за выпавшего в осадок нерастворимого в воде карбоната кальция, однако при дальнейшем пропускании углекислого газа помутнение исчезает в результате образования растворимого гидрокарбоната кальция:
Именно наличием гидрокарбонатов кальция и магния в природной воде и объясняется её временная жёсткость. Почему временная? Потому что при нагревании растворимый гидрокарбонат кальция снова превращается в нерастворимый карбонат:
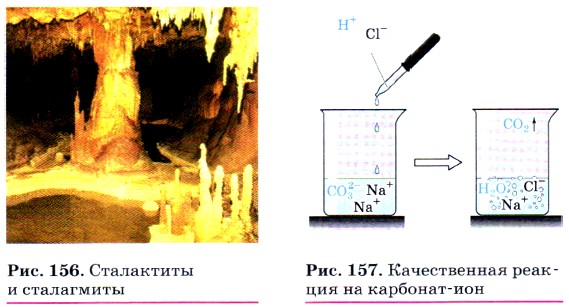
Эта реакция приводит к образованию накипи на стенках котлов, труб парового отопления и домашних чайников. В природе в результате этой реакции в пещерах формируются свисающие вниз причудливые сталактиты, навстречу которым снизу вырастают сталагмиты (рис. 156).
Другие соли кальция и магния, в частности хлориды и сульфаты, придают воде постоянную жёсткость, которую невозможно устранить кипячением. Для удаления солей, вызывающих постоянную жёсткость, приходится использовать другой карбонат — соду Na2CO3, которая переводит ионы Са 2+ в осадок, например:
Соду можно использовать и для устранения временной жёсткости воды.
Карбонаты и гидрокарбонаты можно обнаружить с помощью растворов кислот: при действии на них кислот наблюдается характерное «вскипание» из-за выделяющихся пузырьков углекислого газа (рис. 157):
Эта реакция является качественной на соли угольной кислоты.
1. Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
2. Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока — сделайте сообщение по ключевым словам и словосочетаниям следующего параграфа.
1. Рассмотрите реакцию восстановления оксида железа (III) оксидом углерода (II) как окислительно-восстановительный процесс.
2. Какие несолеобразующие оксиды вам ещё известны, кроме оксида углерода (II)? Верно ли с химической точки зрения другое синонимическое название их — безразличные, или индифферентные, оксиды?
3. Напишите уравнения реакций, характеризующие свойства оксида углерода (IV). Рассмотрите взаимодействие оксида углерода (IV) с магнием как окислительно-восстановительный процесс.
4. Почему раствор углекислого газа окрашивает лакмус в красный цвет? Почему при длительном хранении этого раствора лакмус снова приобретает фиолетовую окраску?
5. Напишите формулы следующих солей: карбоната меди (II), гидрокарбоната меди (II), гидроксокарбоната меди (II). К какой группе солей относится каждая соль? Как ещё называют последнюю соль?
6. Напишите уравнения реакций, с помощью которых можно осуществить превращения:
Рассмотрите процессы окисления-восстановления.
7. В 1060 г 2%-го раствора карбоната натрия растворили 14,3 г кристаллической соды (Na2CO3 • 10Н2O). Вычислите массовую долю соли в полученном растворе. Вычислите объём углекислого газа (н. у.), который образуется при взаимодействии полученного раствора с избытком соляной кислоты.
- Кислородные соединения углерода. Ответы
Источник