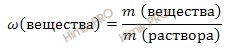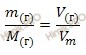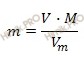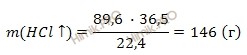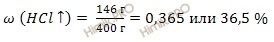Химик.ПРО – решение задач по химии бесплатно
В 254 граммах воды растворили 89,6 литра хлороводорода (HCl↑) (при нормальных условиях). Какова массовая доля хлороводорода (HCl↑) в растворе?
Задачу можно решить, используя формулу нахождения массовой доли растворенного вещества в растворе:
Массовая доля растворенного вещества в растворе – это отношение массы растворенного вещества к массе раствора. Выражается в долях единицы или в %. Следует отметить, что массовая доля растворенного вещества в растворе, выраженная в %, называется процентной концентрацией раствора.
Так как, хлороводород – газообразное вещество, то для нахождения массы 89,6 л хлороводорода будем использовать формулу перерасчета, которая устанавливает связь между массой и объемом газа:
Откуда выразим массу произвольного объема газа:
Учитывая, что молярная масса хлороводорода равна:
M (HCl↑) = 1 + 35,5 = 36,5 (г/моль)
Рассчитаем массу газа:
На заметку: хлороводород – газ с резким запахом, который хорошо растворятся в воде с образованием соляной кислоты (HCl).
Найдем массу раствора, используя формулу нахождения массы раствора:
m (раствора) = 146 + 254 = 400 (г).
Используя формулу нахождения массовой доли растворенного вещества в растворе, вычислим массовую долю хлороводорода в растворе:
Ответ: массовая доля хлороводорода в растворе (HCl) = 0,365 или 36,5 %.
Источник